题目内容
一块表面已被氧化为氧化钠的钠块5.4g,投入50g水中,最多能产生0.10g气体,则原来被氧化的钠是( )
| A.2.3g | B.3.1g | C.4.6g | D.5.3g |
A
解析试题分析:根据钠和水反应生成氢氧化钠与氢气的化学方程式,找到题给的已知量氢气的质量,求得参加反应的钠的质量,再计算出被氧化的钠的质量。
设产生0.10g氢气需钠的质量为x
2Na+2H2O=2NaOH+H2↑
46g 2g
x 0.1g
解得x=2.3g
则氧化钠的质量是5.4g-2.3g=3.1g
则对应的被氧化的钠的质量为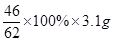 =2.3g
=2.3g
答案选A。
考点:考查关键方程式以及钠被氧化的有关计算
点评:该题是中等难度的试题,侧重对学生答题能力的培养,有利于培养学生的规范答题能力。根据化学方程式计算时,反应物和生成物的质量关系都是纯量,注意解题格式要规范完整,另外本题还要注意审题,被氧化的钠和氧化钠是两码事,不能混淆。

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案
相关题目
用NA表示阿伏加德罗常数的数值,下列说法正确的是
| A.2.3g金属钠与过量的氧气反应,无论加热与否转移电子数均为0.1NA |
| B.1molNa2CO3晶体中含CO32ˉ离子数小于NA |
| C.惰性电极电解食盐水,若线路中通过NA个电子,则阳极产生气体11.2L |
| D.0.1mol的CaO2中含阴离子数是0.2NA |
设NA为阿伏加德罗常数的值,下列有关叙述正确的是
| A.1mol Cl2溶于足量水中转移电子数为NA |
| B.在熔融状态下,1molKHSO4完全电离出的阳离子数为2NA |
| C.标准状况下,22.4LNO与CO2的混合气体中含有的原子数为2NA |
| D.CaC2含有的π键的数目为0.2NA |
下列化学用语正确的是 ( )
| A.1,2—二溴乙烷的结构简式:C2 H4 Br2 |
| B.羟基的化学式:OH- |
| C.己烷的分子式:C6H12 |
| D.乙烯分子的最简式:CH2 |
下列各组物质中分子数相同的是( )
| A.2LCO和2LCO2 |
| B.9gH2O和标准状况下11.2LCO2 |
| C.标准状况下1molO2和22.4LH2O |
| D.0.2molH2和4.48LHCl气体 |
用NA表示阿伏加德罗常数,下列叙述正确的是
| A.2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
| B.0.5molC3H8分子中所含C-H共价键数为2NA |
| C.标准状况下,22.4L乙醇完全燃烧所耗的氧气分子数为3NA |
| D.1mol碳正离子CH5+所含的电子数为11NA |
下列有关化学用语使用正确的是( )
A.CO2的电子式: |
B.核内有8个中子的碳原子: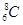 |
C.钾原子结构示意图: |
D.乙烯的比例模型: |
单晶硅是信息产业中重要的基础材料。通常用碳在高温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450~500℃),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。
相关信息如下:
a.四氯化硅遇水极易水解;
b.硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
c.有关物质的物理常数见下表:
| 物质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
| 沸点/℃ | 57.7 | 12.8 | - | 315 | - |
| 熔点/℃ | -70.0 | -107.2 | - | - | - |
| 升华温 度/℃ | - | - | 180 | 300 | 162 |
请回答下列问题:
(1)写出装置A中发生反应的离子方程式_________________________。
(2)装置E中的h瓶需要冷却的理由是_______________________________。
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,除铁元素外可能还含有的元素是________(填写元素符号)。
(4)为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
①滴定前是否要滴加指示剂?________(填“是”或“否”),请说明理由__________________________________。
②某同学称取5.000 g残留物,经预处理后在容量瓶中配制成100 mL溶液,移取25.00 mL试样溶液,用1.000 × 10-2 mol·L-1KMnO4标准溶液滴定。达到滴定终点时,消耗标准溶液20.00mL,则残留物中铁元素的质量分数是_______。