题目内容
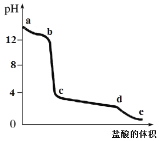
【题目】向偏铝酸钠溶液中逐滴加入盐酸,溶液的pH值随着加入盐酸体积的变化曲线如图所示,则下列说法正确的是
A.a~b段的主要离子方程式为A1O2+4H+=Al3++2H2O
B.向c点溶液中滴加氨水,发生的离子方程式为 A13++3OH=Al(OH)3↓
C.c~d段的主要离子方程式为Al(OH)3+3H+=A13++3H2O
D.向c点溶液中加入碳酸钠,发生的离子方程式为2A13++3CO32+3H2O=2Al(OH)3↓+3CO2↑
【答案】C
【解析】
偏铝酸钠溶液中存在水解平衡AlO2-+2H2OAl(OH)3+OH-,所以溶液显碱性,向溶液中逐滴加入盐酸,a~b段H+先与OH-反应;b~c段pH发生突变,主要发生H+与AlO2-的反应,生成Al(OH)3和NaCl;c~d段盐酸过量后Al(OH)3与盐酸反应,生成AlCl3;
A、a~b段的主要离子方程式为H++OH-═H2O,故A错误;
B、c点Al3+已沉淀完全,加入氨水不发生反应,故B错误;
C、c~d段盐酸过量后,Al(OH)3与盐酸反应,生成AlCl3,故C正确;
D、c点Al3+已沉淀完全,加入Na2CO3溶液不发生反应,故D错误;
故选C。

【题目】汽车尾气中含有CO、NOx等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体。
(1)已知 4CO(g)+2NO2(g)![]() 4CO2(g)+N2(g) ΔH= -1200kJ·mol-1
4CO2(g)+N2(g) ΔH= -1200kJ·mol-1
①该反应在________________(填“高温、低温或任何温度”)下能自发进行。
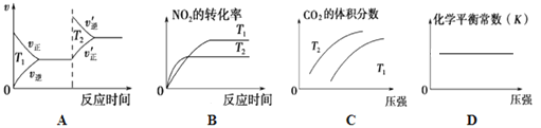
②对于该反应,改变某一反应条件(温度T1>T2),下列图像正确的是_______(填序号)。
③某实验小组模拟上述净化过程,一定温度下,在 2L的恒容密闭容器中,起始时按照甲、乙两种方式进行投料,经过一段时间后达到平衡状态,测得甲中CO的转化率为50%,则该反应的平衡常数为__________;两种方式达平衡时,N2的体积分数:甲______乙( 填“>、=、<或不确定”,下同),NO2的浓度:甲______乙。
甲 | 乙 |
0.2mol NO2 | 0.1mol NO2 |
0.4mol CO | 0.2mol CO |
(2)柴油汽车尾气中的碳烟(C)和NOx可通过某含钴催化剂催化消除。不同温度下,将模拟尾气(成分如下表所示)以相同的流速通过该催化剂测得所有产物(CO2、N2、N2O)与NO的相关数据结果如图所示。
模拟尾气 | 气体(10mol) | 碳烟 | ||
NO | O2 | He | ||
物质的量(mol) | 0.025 | 0.5 | 9.475 | a |
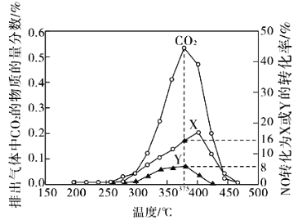
①375℃时,测得排出的气体中含0.45mol O2和0.0525mol CO2,则Y的化学式为________。
②实验过程中采用NO模拟NOx,而不采用NO2的原因是______________________。
【题目】下列各组物质中,物质之间通过一步反应不能实现如图所示转化的是
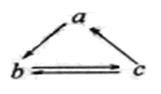
a | b | c | |
A | Al2O3 | Na[Al(OH)4] | Al(OH)3 |
B | HNO3 | NO | NO2 |
C | Si | SiO2 | H2SiO3 |
D | Fe | FeCl3 | FeCl2 |
A.AB.BC.CD.D