题目内容
【题目】某研究性学习小组的同学通过查阅资料知,NO可与炽热的铜粉发生反应,他们设计如下装置(夹持装置略去)进行实验验证。
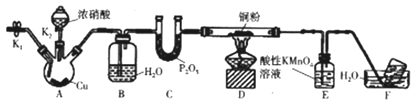
已知:NO能被酸性高锰酸钾溶液氧化生成NO3-。
请回答下列问题:
(1)实验开始前,检查装置气密性的方法是关闭K1、K2,将导管未端置于盛水的水槽中,______________,则表明装置气密性良好;装置A中发生反应的离子方程式为___________________。
(2)装置B的作用为____________________。
(3)装置A中反应开始前,需要先打开K1,向装置中通入一段时间的N2或CO2,其目的是______________________。
(4)实验过程中,装置D中铜粉变黑,装置E中溶液颜色变浅,则装置E中发生反应的离子方程式为_________________________。请设计一种简单的实验方案,证明该离子反应中的氧化产物为NO3-________________________(写出主要的操作过程、现象、结论)。
(5)从绿色化学角度考虑,实验结束后,拆卸装置前,还应进行的一项操作是_________________。
【答案】 用酒精灯微热三颈烧瓶水槽中有气泡产生撤去酒精灯后导管中有一段倒吸的水柱 Cu+2NO3-+4H+=Cu2++ 2NO2↑+ 2H2O 将NO2转化为NO 排除装置内的空气,防止NO 及加热时Cu被空气中的氧气氧化 3MnO4-+5NO+4H+=3Mn2++5NO3-+2H2O 取适量E中溶液放入试管中,加入稀硫酸后再加入铜片,若试管口有红棕色气体生成,则说明有NO3-生成,否则没有NO3-生成 打开K1,向装置内通入一段时间的氮气
【解析】考查实验方案设计与评价,(1)检验气密性,关闭K2、K2,将导管未端置于盛水的水槽中,用酒精灯微热三颈烧瓶水槽中有气泡产生撤去酒精灯后导管中有一段倒吸的水柱,证明气密性良好;装置A制备NO2,发生的离子方程式为 Cu+2NO3-+4H+=Cu2++ 2NO2↑+ 2H2O;(2)实验的目的是用NO与Cu发生反应,即B装置发生的反应是3NO2+H2O=2HNO3+NO,B装置的作用是将NO2转化成NO;(3)因为NO能与O2发生反应生成NO2,加热状态下Cu与O2生成CuO,因此反应开始前通入一段时间的N2或CO2,目的是排尽装置中的空气,防止O2与NO、Cu发生反应;(4)D中铜粉变黑,说明铜与NO发生反应,生成Cu和N2,根据信息NO能与酸性高锰酸钾溶液发生反应,即装置E的目的是除去未反应的NO,即离子反应方程式为3MnO4-+5NO+4H+=3Mn2++5NO3-+2H2O;证明NO3-的存在,NO3-在酸性条件下具有强氧化性,方法是取适量E中溶液放入试管中,加入稀硫酸后再加入铜片,若试管口有红棕色气体生成,则说明有NO3-生成,否则没有NO3-生成 ;(5)反应停止后,装置中还有未反应的NO,NO有毒,必须除去,实验结束后,拆卸装置前,应打开K1,向装置内通入一段时间的氮气,让NO全部被酸性高锰酸钾溶液吸收。

【题目】常温下,向某Ba(OH)2溶液中逐滴加入pH=x的盐酸,测得混合溶液的部分pH如表所示:
序号 | 氢氧化钡溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
① | 22.00 | 0.00 | 13 |
② | 22.00 | 18.00 | 12 |
③ | 22.00 | 22.00 | 7 |
(1)Ba(OH)2溶液的物质的量浓度为?
(2)x的值是多少?
(3)向100mL上述Ba(OH)2溶液中逐滴加入0.05mol/L NaHCO3溶液,当沉淀刚好达最大值时溶液的pH为多少?(已知lg2=0.3)
【题目】气体的自动化检测中常常应用原电池原理的传感器.如图为电池的工作示意图:气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号.下表列出了待测气体及敏感电极上部分反应产物.
待测气体 | 部分电极反应产物 |
NO2 | NO |
Cl2 | HCl |
CO | CO2 |
H2S | H2SO4 |
则下列说法中正确的是( )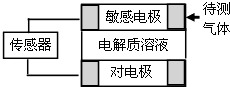
A.上述气体检测时,敏感电极均作电池正极
B.检测Cl2气体时,敏感电极的电极反应为:Cl2+2e﹣═2Cl﹣
C.检测H2S气体时,对电极充入空气,对电极上的电极反应式为O2+2H2O+4e﹣═4OH﹣
D.检测H2S和CO体积分数相同的两份空气样本时,传感器上产生的电流大小相同

