题目内容
11.将23g钠溶于77g水中,所得溶液中溶质的质量分数为( )| A. | 等于23% | B. | 大于23% | C. | 等于40% | D. | 大于40% |
分析 钠投入到水中,发生根据反应的化学方程式分析生成NaOH的质量和溶液的质量,进而计算溶质的质量分数.
解答 解:由于钠是活泼金属能与水发生2Na+2H2O=2NaOH+H2↑的反应,所以反应后生成的溶质设23克金属钠与水反应生成氢氧化钠的质量为X,生成氢气质量为Y:
2Na+2H2O═2NaOH+H2↑
46 36 80 2
23g 18 x y
$\frac{46}{23}=\frac{80}{x}=\frac{2}{y}$,解得x=40g;y=1g,
反应后所得溶液的质量分数:$\frac{40}{23+77-1}×100%$,该值一定大于40%.
故选D.
点评 通过回答本题知道了有的物质放入水中溶质会发生改变,此时的溶质的质量要根据方程式算出再进行计算.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
9.用如图所示的实验装置完成对应的实验(部分仪器已省略),不能达到实验目的是( )
| A. |  制取纯净氢氧化亚铁 | B. | 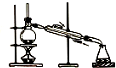 石油的蒸馏 | ||
| C. | 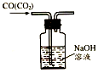 除去CO气体中的CO2气体 | D. | 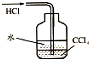 吸收HCl |
16.用10mL 0.1mol/L BaCl2溶液恰好可分别使相同体积的硫酸铁、硫酸锌和硫酸钾三种溶液中的SO42-完全转化为硫酸钡沉淀,则这三种硫酸盐的物质的量浓度之比为( )
| A. | 1:1:3 | B. | 1:2:3 | C. | 1:3:3 | D. | 3:2:2 |
3.能确认水是由氢元素和氧元素组成的实验是( )
| A. | 水的蒸馏 | B. | 水的净化 | C. | 水的蒸发 | D. | 水的电解 |
20.利用红外光谱对有机化合物分子进行测试并记录,可以判断该有机物分子拥有的( )
| A. | 同分异构体数 | B. | 原子个数 | C. | 基团种类 | D. | 相对分子量 |
 X、Y、Z、R、M、Q为前四周期元素,且原子序数依次增大,YZ2是红棕色气体;X与Y元素可形成YX3;R+与Z2-具有相同的核外电子排布;M-的M层电子数是K层上电子的4倍;Q2+离子的3d轨道中有9个电子.
X、Y、Z、R、M、Q为前四周期元素,且原子序数依次增大,YZ2是红棕色气体;X与Y元素可形成YX3;R+与Z2-具有相同的核外电子排布;M-的M层电子数是K层上电子的4倍;Q2+离子的3d轨道中有9个电子.