��Ŀ����
����Ŀ����������ۺ����ü������ڽ�Լ��Դ���������ڱ���������ʵ�������÷Ͼɻ�ͭ��Cu��Zn�Ͻ𣬺���������Fe���Ʊ��������壨CuSO45H2O����������ZnO���Ʊ�����ͼ���£� 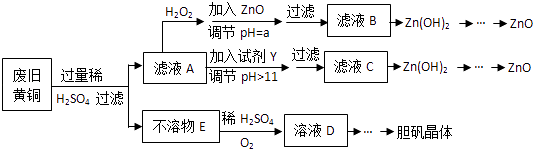
��֪��Zn���������������Al����������������ƣ�pH��11ʱZn��OH��2������NaOH��Һ����[Zn��OH��4]2���±��г��˼������������������������pH����ʼ������pH����������Ũ��Ϊ1.0molL��1���㣩��
Fe3+ | Fe2+ | Zn2+ | |
��ʼ������pH | 1.1 | 5.8 | 5.9 |
������ȫ��pH | 3.0 | 8.8 | 8.9 |
��ش��������⣺
��1������ZnO����pH=a��Ŀ���� �� a�ķ�Χ�� ��
��2���ɲ�����E������ҺD�Ļ�ѧ����ʽΪ ��
��3����ҺA�м���H2O2��Ӧ�����ӷ���ʽΪ ��
��4������ҺD�Ƶ��������������Ҫ���������� ��
��5�������Լ�����ΪY�Լ����� �� A��ZnO B��NaOH C��Na2CO3D��ZnSO4
������ҺC����μ�������ֱ��������������������� ��
���𰸡�
��1��ʹ��Һ�е�Fe3+��ȫ������Zn2+����������3.0��a��5.9
��2��2Cu+O2+2H2SO4=2CuSO4+2H2O
��3��2Fe2++H2O2+2H+=2Fe3++2H2O
��4������Ũ������ȴ�ᾧ������
��5��B���Ȳ�����ɫ����������ܽ�
���������⣺�����̿�֪���Ͼɻ�ͭ��Cu��Zn�Ͻ𣬺���������Fe���Ʊ��������壨CuSO45H2O����������ZnO���Ͼɻ�ͭ�������ϡ������˵õ�������EΪCu����ҺAΪ��������������п����ҺA�м����������������������������Ϊ�����ӣ���������п������ҺPH3.0����5.9������ȫ��������п���Ӳ����������˵õ���Һ�м������Һ����п��������������п�����յõ�����п������ҺA�м�������Լ�YΪ����������Һ����������ȫ�����������˺����Һ��ΪNa2ZnO2 �� �����ᷴӦ����������п���������յõ�����п��������E��ͨ������ͬʱ����ϡ������Һ��Ӧ��������ͭ��Һ������Ũ������ȴ�ᾧ�õ�����ͭ���壻��1������пΪ�������������H+��Ӧ������H+Ũ�ȣ���ʹFe3+����ˮ������ Fe��OH��3��������ȥ�����Դ��ǣ�����H+Ũ�ȣ���ʹFe3+����ˮ������ Fe��OH��3��������ȥ����������ȫ������PH=3.0��п��ʼ������PH=5.9����������̶������ӣ�п���Ӳ�������PHȡֵ��ΧΪ��3.0��a��5.9�����Դ��ǣ�ʹ��Һ�е�Fe3+��ȫ������Zn2+����������3.0��a��5.9����2����Ϊ������������Һ���Ȱ�ͭ����������ͭ����Ȼ����һ�����ķ�Ӧ���γ�һ��ƽ�⣬�����γɵ�����ͭ���Ͼͻᱻϡ�����ܽ⣬ƽ�ⱻ���ƣ���Ӧ����������У��ʶ����ܽ⣬��Ӧ�Ļ�ѧ����ʽΪ��2Cu+O2+2H2SO4=2CuSO4+2H2O��
���Դ��ǣ�2Cu+O2+2H2SO4=2CuSO4+2H2O����3����ҺA����Ҫ���������������������¹���������������ԣ������������������������ӣ����ӷ�ӦΪ2Fe2++H2O2+2H+=2Fe3++2H2O��
���Դ��ǣ�2Fe2++H2O2+2H+=2Fe3++2H2O����4������ҺD�Ƶ��������Ǵ���Һ�еõ����壬ʵ�������Ҫ����Ũ������ȴ�ᾧ�Լ����˵Ȳ��������Դ��ǣ�����Ũ������ȴ�ᾧ�����ˣ���5��Zn���������������Al����������������ƣ�������п�������ԣ�pH��11ʱ��Zn��OH��2������NaOH��Һ����[Zn��OH��4]2�� �� �˹�����Ҫ����pHֵ����11���ʿ��Լ���ǿ��NaOH��Һ��Ȼ�������������������п���������������ᣬ�����ܽ⣬
���Դ��ǣ�B���Ȳ�����ɫ�������ܽ⣮

 100�ִ�����ĩ���ϵ�д�
100�ִ�����ĩ���ϵ�д� ��У���˿��ֿ���ϵ�д�
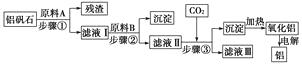
��У���˿��ֿ���ϵ�д�����Ŀ�����̿����Ҫ�ɷ�ΪMnO2 �� ������Al2O3��SiO2����п����Ҫ�ɷ�ΪZnS��������FeS��CuS��CdS���ʡ��������̿����п��Ϊԭ���Ʊ�MnO2��Zn������������£��м����Ĺ��岿���Ѿ���ȥ����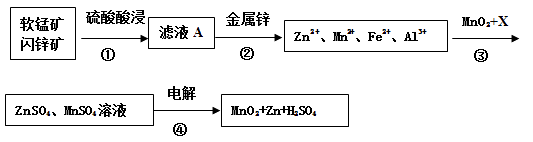
��֪�� ��ʯ�����н���Ԫ������ҺA�о���������ʽ���ڡ�
���ֽ���������ȫ������pH���±���
Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
�ش��������⣺
��1���������Ϊ�˼ӿ�����Ľ�ȡ���ʣ��ɲ��õķ���������дһ�֣������з��������Ӧ������MnO2��FeS�����Ṳ��ʱ�е���ɫ������������Һ��Ϊ�ػ�ɫ��д��MnO2��FeS�����Ṳ�ȷ�����Ӧ�Ļ�ѧ����ʽ��
��2������ڼ������п��Ϊ�˻��ս��������ս�������Ҫ�ɷ�����
��3���������MnO2�������� ������һ������X������ ��
A.ZnO B.MgCO3 C. MnCO3 D.Cu(OH)2
��4��MnO2��Li����LiMnO2 �� ������Ϊij����ӵ�ص��������ϣ���ط�Ӧ����ʽΪ�� Li1-xMnO2+LixC6=LiMnO2+6C��д��������ӵ�ص������缫��Ӧʽ��
��5����֪��HCN�ĵ��볣��K=4.9��10��10 �� H2S�ĵ��볣��K1=1.3��10�D7 �� K2=7.0��10�D15 �� ��NaCN��Һ��ͨ��������H2S���壬��Ӧ�����ӷ���ʽΪ���ڷ�ˮ���������г���H2S��Mn2+ת��ΪMnS��ȥ������0.020 mol��L-1Mn2+��ˮ��ͨ��һ������H2S���壬������Һ��pH=a����HS�DŨ��Ϊ1.0��10�D4 mol��L-1ʱ��Mn2+��ʼ��������a=��[��֪��Ksp(MnS)=1.4��10�D15]