题目内容
下列反应中旧化学键断裂吸收的总能量大于新化学键形成放出总能量的是
| A.电解水制取H2和O2 | B.甲烷燃烧 |
| C.铝粉与氧化铁粉末反应 | D.油脂在人体内完全氧化生成CO2和H2O |
A
解析试题分析:反应中旧化学键断裂吸收的总能量大于新化学键形成放出总能量,这说明该反应是吸热反应,因此选项A正确,其余选项都是放热反应,答案选A。
考点:考查放热反应与吸热反应的判断

练习册系列答案
相关题目
如下图所示,△H1=-393.5 kJ?mol-1,△H2=-395.4 kJ?mol-1,下列说法或表示式正确的是( )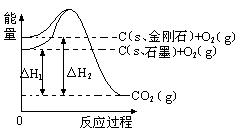
| A.C(s、石墨)=C(s、金刚石) △H="+1.9" kJ?mol-1 |
| B.石墨和金刚石的转化是物理变化 |
| C.金刚石的稳定性强于石墨 |
| D.1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ |
下列说法正确的是( )
A.如图可表示水分解过程中的能量变化 |
| B.若2C(s)+O2(g)=2CO(g)△H="-221.0" kJ/mol,则碳的燃烧热为110.5 kJ/mol |
| C.需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应 |
| D.已知:Ⅰ:对于反应:H2(g)+Cl2(s)="2HCl" (g)△H="-" a kJ/mol, |

且a、b、c均大于零,则断开1molH-Cl键所需的能量为- a-b-c
化学能与热能、电能等能相互转化。关于化学能与其他能量相互转化的说法正确的是
| A.化学反应中能量变化的主要原因是化学键的断裂与生成 |
| B.铝热反应中, 反应物的总能量比生成物的总能量低 |
| C.图I所示的装置能将化学能转变为电能 |
| D.图II所示的反应为吸热反应 |
中和热测定实验中,通过简易量热计直接测得的数据是
| A.反应的热量变化 | B.体系的温度变化 |
| C.酸或碱的浓度变化 | D.生成水的物质的量 |
下图表示某可逆反应在使用和未使用催化剂时,反应过程和能量的对应关系。下列说法一定正确的是 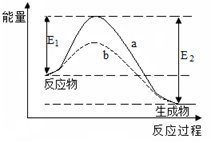
| A.该反应为吸热反应 |
| B.反应物吸收的总能量小于形成生成物释放的总能量 |
| C.a与b相比,反应的平衡常数一定不同 |
| D.a与b相比,a的反应速率更快 |
2HI(g)  H2(g)+I2(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是
H2(g)+I2(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是
| A.该反应为放热反应 |
| B.升高温度,不影响活化分子百分数 |
| C.催化剂能降低该反应的活化能 |
| D.逆反应的活化能等于正反应的活化能 |
下列反应既是氧化还原反应,又是吸热反应的是( )
| A.实验室制备氢气 | B.Ba(OH)2·8H2O与NH4Cl的反应 |
| C.灼热的碳与水的反应 | D.铝粉与氧化铁粉末反应 |
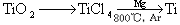
 CO2(g); ΔH=-395.5 kJ·mol-1
CO2(g); ΔH=-395.5 kJ·mol-1