题目内容
2.对于H2在O2中燃烧反应的描述,正确的是( )| A. | 该反应属于放热反应 | B. | 断开H-H键放出能量 | ||
| C. | 形成O-H键吸收能量 | D. | 反应后生成物总能量升高 |
分析 A.燃烧反应为放热反应;
B.断键吸收能量;
C.成键放出能量;
D.放热反应生成物的总能量小于反应物的总能量.
解答 解:A.H2在O2中燃烧反应为放热反应,故A正确;
B.断裂H-H键需要吸收能量,故B错误;
C.生成H-O键会放出能量,故C错误;
D.放热反应生成物的总能量小于反应物的总能量,所以反应后生成物总能量降低,故D错误;
故选A.
点评 本题考查化学反应的热量变化,学生应注重归纳中学化学中常见的吸热或放热的反应,对于特殊过程中的热量变化的要熟练记忆来解答此类习题.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
20.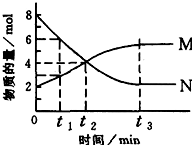 在一定温度下,某容器内某一反应中,M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,某容器内某一反应中,M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
 在一定温度下,某容器内某一反应中,M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,某容器内某一反应中,M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A. | 此反应为不可逆反应 | B. | t2时,正逆反应速率相等,达到平衡 | ||
| C. | t3时,正反应速率大于逆反应速率 | D. | t3时,正反应速率等于逆反应速率 |
1.下列说法不正确的是( )
| A. | 我国最早使用的合金是由铜锌合金制成的青铜器 | |
| B. | 储氢合金是一类能大量吸收H2,并与H2结合成金属氢化物的材料 | |
| C. | 一般汽车配件中的发动机使用的是密度小、强度大且耐腐蚀的铝合金材料 | |
| D. | 钛合金,形状记忆合金,耐热合金以及储氢合金都属于新型合金 |
7.把500mL含有BaCl2和KCl的混合溶液分成5等份,取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含b mol硝酸银的溶液,恰好使氯离子完全沉淀.则该混合溶液中钾离子浓度为( )
| A. | 0.1(b-2a)mol•L-1 | B. | 10(2a-b)mol•L-1 | C. | 10(b-a)mol•L-1 | D. | 10(b-2a)mol•L-1 |
14.向含有等物质的量的NH4+、Al3+、H+混合溶液中,慢慢滴加NaOH溶液,直至过量,发生以下离子反应:①H++OH-═H2O ②Al(OH)3+OH-═AlO2-+2H2O ③Al3++3OH-═Al(OH)3↓④NH4++OH-═NH3•H2O.发生反应的先后顺序正确的是( )
| A. | ①→④→③→② | B. | ①→③→②→④ | C. | ①→③→④→② | D. | ①→②→③→④ |
12.下列有关甲苯的事实中,能说明侧链对苯环性质有影响的是( )
| A. | 甲苯燃烧时产生很浓的黑烟 | |
| B. | 甲苯通过硝化反应可生成三硝基甲苯 | |
| C. | 甲苯能使酸性高锰酸钾溶液褪色 | |
| D. | 1mol甲苯与3mol氢气发生加成反应 |
 =2Cr(OH)3↓+3O2↑+2H2O.
=2Cr(OH)3↓+3O2↑+2H2O.