题目内容
【题目】高炉炼铁过程中发生的主要反应为:![]() Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)![]()
![]() Fe(s)+CO2(g)。已知该反应在不同温度下的平衡常数如下:
Fe(s)+CO2(g)。已知该反应在不同温度下的平衡常数如下:
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
请回答下列问题:
(1)该反应的平衡常数表达式K=________,该反应是_________反应(填“放热”或“吸热”)。
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe2O3、CO各4.0 mol,反应经过20min后达到平衡。求该时间范围内反应的平均反应速率v(CO)=__________、CO的平衡转化率=__________。
(3)欲提高(2)中CO的平衡转化率,可采取的措施是________
A.降低反应温度 B.增加Fe2O3的量 C.加入合适的催化剂 D.移出部分CO2 E.减小容器的容积
(4)在1L的密闭容器中,1150℃条件,下列达平衡状态的是__________。
A | B | C | D | |
n(Fe2O3) | 0.350 | 0.027 | 0.080 | 0.080 |
n(CO) | 0.010 | 0.010 | 0.010 | 0.050 |
n(Fe) | 0.100 | 0.064 | 0.080 | 0.080 |
n(CO2) | 0.035 | 0.088 | 0.037 | 0.050 |
【答案】![]() 放热 0.016mol/(Lmin) 80% AD C
放热 0.016mol/(Lmin) 80% AD C
【解析】
(1)反应![]() Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)![]()
![]() Fe(s)+CO2(g)的平衡常数
Fe(s)+CO2(g)的平衡常数![]() ;由表中数据可知,温度越高平衡常数越小,故升高温度平衡向逆反应移动,正反应为放热反应;
;由表中数据可知,温度越高平衡常数越小,故升高温度平衡向逆反应移动,正反应为放热反应;
(2)令平衡时CO的物质的量变化为nmol,则:
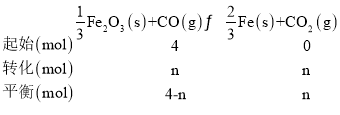
![]() ,解得n=3.2,所以
,解得n=3.2,所以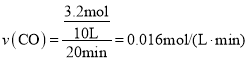 ,CO的平衡转化率为
,CO的平衡转化率为![]() ;
;
(3)A.降低反应温度,平衡将正向移动,可提高CO的平衡转化率,故A符合题意;
B.氧化铁是固体,增加Fe2O3的量,不影响平衡移动,CO的平衡转化率不变,故B不符合题意;
C.加入合适的催化剂,平衡不移动,故C不符合题意;
D.移出部分CO2,平衡向正反应移动,CO的平衡转化率增大,故D符合题意;
E.反应前后气体的物质的量不变,减小容器的容积,增大压强平衡不移动,CO的平衡转化率不变,故E不符合题意;
故答案为:AD;
(4)1150℃下,平衡常数K=3.7;
A.浓度商![]() ,反应未达到平衡状态,故A不符合;
,反应未达到平衡状态,故A不符合;
B.浓度商![]() ,反应未达到平衡状态,故B不符合;
,反应未达到平衡状态,故B不符合;
C.浓度商![]() ,反应达到平衡状态,故C符合;
,反应达到平衡状态,故C符合;
D.浓度商![]() ,反应未达到平衡状态,故D不符合;
,反应未达到平衡状态,故D不符合;
故答案为:C。

 科学实验活动册系列答案
科学实验活动册系列答案