题目内容
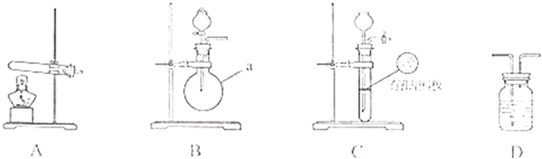
下图中甲、乙两个装置用导线连接,有关叙述正确的是

- A.甲装置中Cu为阳极,乙装置Fe为负极
- B.甲装置中SO2-4向Cu极移动,乙装置中的Na+向石墨极移动
- C.乙烧杯中Fe极的电极反应式为:2H2O+2e-=2OH-+H2↑
- D.当石墨电极上产生11.2L(标准状况)气体时,消耗Zn的质量为65g
C
左边容易自发进行是原电池,锌作负极、铜作正极,右边是电解池铁作阴极、石墨作阳极。甲装置中硫酸根离子向锌电极移动补充负电荷,乙装置中电场力的作用下向铁电极移动。铁电极周围聚集了钠离子和水电离出的氢离子,氢离子先放电生成氢气,石墨电极周围聚集了氢氧根离子和氯离子,氯离子先放电生成氯气,当生成标况下11.2L氯气时转移1mol电子,将有0.5mol锌参加反应质量为32.5 g。
左边容易自发进行是原电池,锌作负极、铜作正极,右边是电解池铁作阴极、石墨作阳极。甲装置中硫酸根离子向锌电极移动补充负电荷,乙装置中电场力的作用下向铁电极移动。铁电极周围聚集了钠离子和水电离出的氢离子,氢离子先放电生成氢气,石墨电极周围聚集了氢氧根离子和氯离子,氯离子先放电生成氯气,当生成标况下11.2L氯气时转移1mol电子,将有0.5mol锌参加反应质量为32.5 g。

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目