��Ŀ����
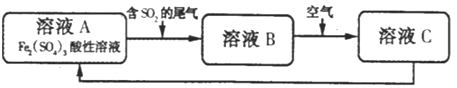
����Ŀ��ij���ε�طŵ�ʱ�Ļ�ѧ����ʽΪ��2K2S2+KI3=K2S4+3KI���������豸���ӵĵ�·��ͼʾ�����պϿ���Kʱ��X������Һ�ȱ�죮������˵����ȷ���ǣ� ��

A. K+���ҵ���ͨ�����ӽ���Ĥ
B. A�ĵ缫��ӦʽΪ��3I����2e��=I3��
C. ����0.1 mol K+ͨ�����ӽ���Ĥ��X�缫�ϲ�����״��������1.12 L
D. ��س��ʱ��B�缫Ҫ�����Դ�������������缫�Ϸ�����ԭ��Ӧ
���𰸡�C
��������
����պϿ���Kʱ���²�����һ�����أ����NaCl��Һ��X������Һ�ȱ�죬��H+��X�ŵ磬��X��������Y�����������ɴ�֪��A�Ǹ�����B��������ԭ������������������ƶ�����K+��B���ƶ���A����A�Ǹ�����Ԫ�صĻ��ϼ����ߣ��ӷ���ʽ�е�Ԫ�ػ��ϼ۵ĸı���������K2S2�ڸ�����Ӧ��B����X��������2H++2e-��H2��, ��0.1 mol K��ͨ�����ӽ���Ĥʱת�Ƶ���Ϊ0.1mol������H2Ϊ0.05mol�����Ϊ1.12L��C�ԣ���س��ʱ��B�缫Ҫ�����Դ�������������缫�Ϸ���������Ӧ��D����

����Ŀ�����³�ѹ�£������ݻ���ͬ����ƿ�зֱ�ʢ��X��Y�������壬����a��ʹ����ƿ�ڵ�������ͨ����������ڵ�ѹǿ�ɴ�С��˳��������ȷ����

��� | �� | �� | �� | �� |
����X | HI | NH3 | H2 | NO |
����Y | Cl2 | HCl | Cl2 | O2 |
A. �������������� B. ��������������
C. �������������� D. ��������������