题目内容
1.X、Y、Z是三种短周期元素.已知三种元素的原子序数按X、Y、Z的顺序依次增大,且原子序数之和为33,最外层电子数之和为11.在周期表中,X、Z上下相邻,Y、Z左右相邻.(1)X、Y、Z的元素符号分别为C、Al、Si.
(2)Y的氧化物是两性氧化物.
(3)X和Z分别能与氧形成XO2和ZO2,XO2在固态时属于分子晶体,ZO2在固态时属于原子晶体.
分析 X、Y、Z是三种短周期元素,三种元素的原子序数按X、Y、Z的顺序依次增大,在周期表中,X、Z上下相邻,Y、Z左右相邻,令Y最外层电子数为a,则X、Z原子最外层电子数为a+1,故a+a+1+a+1=11,解得a=3,即Y处于ⅢA族,X、Z处于ⅣA族,且原子序数之和为33,则Y为Al、X为C、Z为Si,据此解答.
解答 解:(1)X、Y、Z是三种短周期元素,三种元素的原子序数按X、Y、Z的顺序依次增大,在周期表中,X、Z上下相邻,Y、Z左右相邻,令Y最外层电子数为a,则X、Z原子最外层电子数为a+1,故a+a+1+a+1=11,解得a=3,即Y处于ⅢA族,X、Z处于ⅣA族,且原子序数之和为33,则Y为Al、X为C、Z为Si,
故答案为:C;Al;Si;
(2)Y的氧化物是氧化铝,属于两性氧化物,故答案为:两;
(3)X和Z分别能与氧形成CO2和SiO2,CO2在固态时属于分子晶体,SiO2在固态时属于原子晶体,故答案为:分子;原子.
点评 本题考查结构与位置关系,根据位置关系结合最外层电子数或原子序数即可推断元素,注意对基础知识的理解掌握.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
12.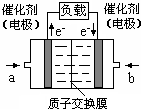 可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如下.甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一电极后与氧气反应,电池总反应为:2CH3OH+3O2=2CO2+4H2O.下列说法不正确的是( )
可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如下.甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一电极后与氧气反应,电池总反应为:2CH3OH+3O2=2CO2+4H2O.下列说法不正确的是( )
 可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如下.甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一电极后与氧气反应,电池总反应为:2CH3OH+3O2=2CO2+4H2O.下列说法不正确的是( )
可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如下.甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一电极后与氧气反应,电池总反应为:2CH3OH+3O2=2CO2+4H2O.下列说法不正确的是( )| A. | 右电极为电池正极,b处通入的物质是空气 | |
| B. | 左电极为电池负极,a处通入的物质是空气 | |
| C. | 负极反应式为:CH3OH+H2O-6e-=CO2+6H+ | |
| D. | 正极反应式为:O2+4H++4e-=2H2O |
9.下列有关胶体和溶液的比较中,正确的是( )
| A. | 溶液中溶质粒子不带电,胶体分散质粒子带电 | |
| B. | 溶液中溶质的粒子运动有规律,胶体粒子运动无规律 | |
| C. | 通直流电后,溶液中溶质的粒子分别向两极运动,而胶体中分散质的粒子向某一极运动 | |
| D. | 溶液中通过一束光线没有特殊现象,胶体中通过一束光线出现光亮的“通路” |
16.在室温下,由水电离出的C(H+)=10-12mol/L的溶液中,下列离子组可大量共存的是( )
| A. | K+、ClO-、SO42-、I- | B. | S2-、SO32-、Na+、K+ | ||
| C. | Fe2+、NO3-、Cl-、K+ | D. | AlO2-、MnO4-、Fe2+、Na+ |
6.根据下列反应判断有关物质还原性由强到弱的顺序是( )
H2SO3+I2+H2O═2HI+H2SO4 2FeCl3+2HI═2FeCl2+2HCl+I2
3FeCl2+4HNO3═2FeCl3+NO↑+2H2O+Fe(NO3)3.
H2SO3+I2+H2O═2HI+H2SO4 2FeCl3+2HI═2FeCl2+2HCl+I2
3FeCl2+4HNO3═2FeCl3+NO↑+2H2O+Fe(NO3)3.
| A. | NO>FeCl2>H2SO3>HI | B. | HI>FeCl2>H2SO3>NO | ||
| C. | FeCl2>HI>H2SO3>NO | D. | H2SO3>HI>FeCl2>NO |
13.下列操作不正确的是( )
| A. | 配制物质的量浓度的溶液,在定容时滴加蒸馏水超过刻度线,可用滴管吸出一部分使其溶液的凹液面与刻度线相切 | |
| B. | 过滤的时候,用玻璃棒引流,并将玻璃棒与三层滤纸的边缘接触 | |
| C. | 试管中滴加溶液时,不能将滴管伸入试管口内,应悬空滴入 | |
| D. | 蒸发氯化钠溶液,待蒸发皿中有大量固体出现时,停止加热,用余热蒸干 |
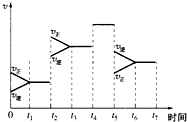 有A气体和B气体在一定条件下在一密闭容器中发生如下反应:A(g)+3B(g)?2C(g)△H<0
有A气体和B气体在一定条件下在一密闭容器中发生如下反应:A(g)+3B(g)?2C(g)△H<0