题目内容
4.下列说法正确的是( )| A. | 离子化合物中只能含离子键,不能有共价键 | |
| B. | 非金属元素之间形成的化学键一定是共价键 | |
| C. | 电子数相同的两种微粒一定是同一元素 | |
| D. | 化学键被破坏的变化不一定是化学变化 |
分析 A、离子化合物中也可能含有共价键;
B、铵盐中全部为非金属元素,但含有离子键;
C、电子数相同的微粒可能为离子、原子、分子等;
D、化学反应的实质为旧键断裂和新键生成.
解答 解:A、离子化合物中也可能含有共价键,如NaOH等,故A错误;
B、铵盐中全部为非金属元素,但铵根离子与酸根离子之间以离子键结合,故B错误;
C、电子数相同的微粒可能为离子、原子、分子等,如HF、Ne、Na+都为10电子微粒,则不一定为同种元素,故C错误;
D、化学反应的实质为旧键断裂和新键生成,则判断化学变化的可靠方法是看有无化学键的变化,如氯化钠溶于水是离子键破坏,是物理变化,故D正确;
故选D.
点评 本题考查化学键,明确化学键的形成及特例是解答本题的关键,学生应学会利用举例的方法来解答.

练习册系列答案
相关题目
14. 分类方法在化学学科的发展中起了非常重要的作用.如图是某反应在密闭容器中反应前后的分子状况示意图,“
分类方法在化学学科的发展中起了非常重要的作用.如图是某反应在密闭容器中反应前后的分子状况示意图,“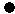 ”和“
”和“ ”分别表示不同的原子.对此反应的分类一定不正确的是( )
”分别表示不同的原子.对此反应的分类一定不正确的是( )
 分类方法在化学学科的发展中起了非常重要的作用.如图是某反应在密闭容器中反应前后的分子状况示意图,“
分类方法在化学学科的发展中起了非常重要的作用.如图是某反应在密闭容器中反应前后的分子状况示意图,“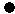 ”和“
”和“ ”分别表示不同的原子.对此反应的分类一定不正确的是( )
”分别表示不同的原子.对此反应的分类一定不正确的是( )| A. | 置换反应 | B. | 氧化还原反应 | C. | 放热反应 | D. | 化合反应 |
15.下列对化学反应的认识不正确的是( )
| A. | 化学反应过程中,一定有新物质生成 | |
| B. | 化学反应过程中,一定有化学键的断裂和形成 | |
| C. | 化学反应过程中,一定有能量的变化 | |
| D. | 如果某化学反应的△H和△S均小于0,则该反应一定能自发进行 |
12.下列叙述合理的是( )
| A. | 金属氧化物是碱性氧化物,酸性氧化物都不能与酸反应 | |
| B. | 明矾[KAl(SO4)2•12H2O]在水中能形成Al(OH)3胶体,可用作净水剂 | |
| C. | ClO2气体中氯元素显+4价,具有强氧化性,其消毒效率(单位体积气体得到电子的数目)是Cl2的5倍 | |
| D. | 雷雨过后感觉空气清新是因为在闪电时发生反应:N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO,使空气中含有一定量的NO |
9.在一个体积固定的密闭容器中,进行的可逆反应A(s)+3B(g)?3C (g).下列叙述中表明可逆反应一定达到平衡状态的是( )
①C的生成速率与C的分解速率相等; ②单位时间内生成amol A,同时生成3amol B;
③B的浓度不再变化; ④混合气体总的物质的量不再发生变化;
⑤A、B、C的物质的量之比为1:3:3; ⑥混合气体的密度不再变化;
⑦B的生成速率与C的生成速率之比为1:1.
①C的生成速率与C的分解速率相等; ②单位时间内生成amol A,同时生成3amol B;
③B的浓度不再变化; ④混合气体总的物质的量不再发生变化;
⑤A、B、C的物质的量之比为1:3:3; ⑥混合气体的密度不再变化;
⑦B的生成速率与C的生成速率之比为1:1.
| A. | ①②③⑦ | B. | ①③④⑥⑦ | C. | ①③⑥⑦ | D. | ①③④⑤⑦ |
13.下列叙述错误的是( )
| A. | SO2、SO3都是极性分子 | |
| B. | 元素电负性越大的原子,吸引电子能力越强 | |
| C. | 非极性键可以存在于化合物中 | |
| D. | 离子化合物的熔点不一定比共价化合物的高 |
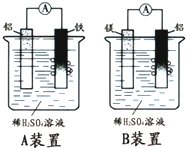 有甲、乙两位学生分别利用如图A、B装置的原电池反应检测金属的活动性顺序,
有甲、乙两位学生分别利用如图A、B装置的原电池反应检测金属的活动性顺序,