题目内容
【题目】若定义pc是溶液中微粒物质的量浓度的负对数,则常温下,一定浓度的某酸(H2A)水溶液中pc(H2A)、pc(HA-)、pc(A2-)随着溶液pH的变化曲线如图所示。下列说法一定正确的是( )
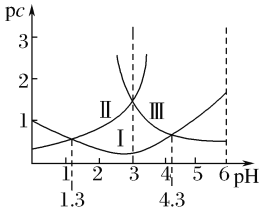
A.pH=4时,c(HA-)<c(A2-)
B.c(H2A)+c(HA-)+c(A2-)是定值
C.常温下,该酸的电离常数Ka1=10-1.3
D.常温下,NaHA的水溶液呈碱性
【答案】C
【解析】
随pH增大,c(H2A)减小、c(HA-)先增后减、c(A2-)增大;根据图示,曲线Ⅰ表示c(HA-)、曲线Ⅱ表示c(H2A)、曲线Ⅲ表示c(A2-);
A、根据图示,pH=4时,c(HA-)>c(A2-),故A错误;
B、调节溶液pH的方法不确定,所以c(H2A)+c(HA-)+c(A2-)不一定是定值,故B错误;
C、根据图示c(H2A)=c(HA-)时,pH=1.3,所以Ka1=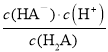 =c(H+)=10-1.3,故C正确;
=c(H+)=10-1.3,故C正确;
D、根据图示c(A2-)=c(HA-)时,pH=4.3,Ka2=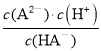 =c(H+)=10-4.3,HA-的水解常数Kh=
=c(H+)=10-4.3,HA-的水解常数Kh=![]() =10-12.7,电离大于水解,所以NaHA的水溶液呈酸性,故D错误。
=10-12.7,电离大于水解,所以NaHA的水溶液呈酸性,故D错误。

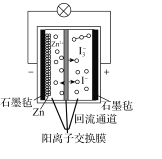
【题目】滴定法是解决化学分析问题的常用方法。滴定的方法有酸碱中和滴定、氧化还原滴定、沉淀滴定、络合滴定等。
I.如图为某浓度的NaOH溶液滴定10.00mL一定浓度的盐酸的示意图。根据图像

(1)HCl溶液的浓度是__________;NaOH溶液的浓度是_______;
(2)x=________。
(3)若向20mL稀氨水中逐滴加入等浓度的盐酸,则下列变化趋势正确的是________(填字母)。


ΙΙ.氧化还原滴定实验与中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。
(4)人体血液里Ca2+的浓度一般采用mg/cm3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度,抽取血样20.00mL,经过上述处理后得到草酸,再用0.020mol/L KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00mL KMnO4溶液。
滴定的实验数据如下所示:
实验编号 | 待测血液的体积/mL | 滴入KMnO4溶液的体积/mL |
1 | 20.00 | 11.95 |
2 | 20.00 | 13.00 |
3 | 20.00 | 12.05 |
①滴定时,盛放高锰酸钾溶液的仪器名称为_________确定反应达到终点的现象_____________。
②草酸跟酸性KMnO4溶液反应的离子方程式为:2MnO42-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O,根据所给数据计算血液样品中Ca2+离子的浓度为__________mg/cm3
【题目】以低品位红土镍矿(主要成分可表示为![]() 、
、![]() 、
、![]() ,含有少量
,含有少量![]() 、
、![]() 、
、![]() 、
、![]() )为原料制备纳米级
)为原料制备纳米级![]() 的工艺流程如下:
的工艺流程如下:

已知氢氧化物的参数如下表:
氢氧化物 | 溶度积 | 开始沉淀 | 完全沉淀 |
|
| 4.1 | 5.5 |
|
| 2.2 | 3.5 |
|
| 6.7 | 9.5 |
|
| 9.4 | 12.4 |
回答下列问题:
(1)“滤渣Ⅰ”的主要成分是______(填化学式)。
(2)常温下,调![]() 的目的是______。当
的目的是______。当![]() 时,溶液中
时,溶液中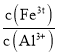 =______
=______
(3)写出“除铜镍”过程发生反应的离子方程式为![]() 、______________。“除钙”过程反应温度不宜超过
、______________。“除钙”过程反应温度不宜超过![]() 的原因_________________________。
的原因_________________________。
(4)“滤液”中溶质的主要成分为________________,获取该物质晶体的具体实验操作为__________。