题目内容
【题目】现有如下药品和装置:质量为w(w<1g)的锌片、稀H2SO4、无水硫酸铜和蒸馏水,设计一个简单实验,测定Zn的相对原子质量(气体体积均可认为是在标准状况下测定)如图 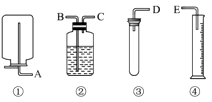
(1)该反应的离子方程式为
(2)应选用的装置的连接顺序是(填接口字母)
(3)操作中,怎样加放试剂以保证不漏出氢气
(4)以下是测量收集气体体积必须包括的几个步骤,则这三步操作的正确顺序是
①调整量筒内外液面调试使之相同
②使试管和量筒内气体都冷却至室温
③读取量筒内气体的体积.
(5)若④中收集到水VmL,则锌的相对原子质量的数学表达式为
(6)由于锌片可能含不溶性杂质,实验测得的锌的相对原子质量可能比真实值(填“偏高”或“偏低”,下同); 若装置气密性不太好,测得值 .
【答案】
(1)Zn+2H+=Zn2++H2↑
(2)DCBE
(3)连接好装置后,打开③的活塞,加入适量的稀硫酸,将试管倾斜一定角度,将锌片放在试管壁上,塞好塞子,缓慢竖起试管将锌片滑入硫酸中,使反应开始
(4)②①③
(5)![]()
(6)偏高;偏高
【解析】解:(1)发生的反应即锌和稀硫酸的反应,离子方程式为:Zn+2H+=Zn2++H2↑,故答案为:Zn+2H+=Zn2++H2↑;(2)将稀硫酸与锌片在③中充分反应,产生的氢气从D通入C,通过B将集气瓶中的水排入量筒中,通过测量排出的水的量来得知产生氢气的量,故装置的连接顺序为:DCBE,故答案为:DCBE;(3)操作中,要保证不漏出氢气,则在塞紧活塞前不让锌和硫酸接触,具体操作为:连接好装置后,打开③的活塞,加入适量的稀硫酸,将试管倾斜一定角度,将锌片放在试管壁上,塞好塞子,缓慢竖起试管将锌片滑入硫酸中,使反应开始,故答案为:连接好装置后,打开③的活塞,加入适量的稀硫酸,将试管倾斜一定角度,将锌片放在试管壁上,塞好塞子,缓慢竖起试管将锌片滑入硫酸中,使反应开始;(4)要准确测量气体体积必须保持量筒内外气体的温度和压强相等,因此在读取量筒内气体的体积之前,应使试管和量筒内的气体都冷却至室温;再调节量筒内外液面高度使之相同,所以正确的顺序为:②①③;
故答案为:②①③;(5)根据提供的数据可知产生的氢气的量为VmL,即生成的氢气的物质的量n= ![]() =
= ![]() mol,而根据反应可知,1mol锌~1mol氢气,故反应掉的锌的物质的量n=
mol,而根据反应可知,1mol锌~1mol氢气,故反应掉的锌的物质的量n= ![]() mol,由于相对原子质量在数值上等于摩尔质量,而锌的摩尔质量M=
mol,由于相对原子质量在数值上等于摩尔质量,而锌的摩尔质量M= ![]() =
= ![]() =
= ![]() g/mol,故锌的相对原子质量为
g/mol,故锌的相对原子质量为 ![]() ,
,
故答案为: ![]() ;(6)由于摩尔质量M=M=
;(6)由于摩尔质量M=M= ![]() =
= ![]() g/mol,假如锌片含不与酸反应的杂质,则测得生成的氢气的体积v偏小,则M偏高;若气密性不好,则测得生成的氢气的体积v偏小,则M偏高,故答案为:偏高,偏高.
g/mol,假如锌片含不与酸反应的杂质,则测得生成的氢气的体积v偏小,则M偏高;若气密性不好,则测得生成的氢气的体积v偏小,则M偏高,故答案为:偏高,偏高.
通过所提供的药品和仪器可知,实验原理为:将稀硫酸与锌片在③中充分反应,产生的氢气从D通入C,通过B将集气瓶中的水排入量筒中,通过测量排出的水的量来得知产生氢气的量,据此分析.(1)发生的反应即锌和稀硫酸的反应;(2)根据实验原理来分析仪器的连接顺序;(3)保证不漏出氢气即保证在塞紧活塞前不让锌和硫酸接触;(4)从气体的热胀冷缩和读量筒中气体体积的方法两方面进行分析;(5)根据提供的数据可知产生的氢气的量,再根据相对原子质量在数值上等于摩尔质量,而摩尔质量M= ![]() 来计算;(6)根据摩尔质量M=
来计算;(6)根据摩尔质量M= ![]() ,通过分析各种操作失误对所测量的氢气体积的影响来分析.
,通过分析各种操作失误对所测量的氢气体积的影响来分析.

【题目】如图表示的一些物质或概念间的从属关系中,不正确的是( )
X | Y | Z | |
例 | 氧化物 | 化合物 | 纯净物 |
A | 苯的同系物 | 芳香烃 | 芳香族化合物 |
B | 烯烃 | 不饱和烃 | 烃 |
C | 氯乙烷 | 卤代烃 | 烃的衍生物 |
D | 加聚反应 | 加成反应 | 化合反应 |

A.A
B.B
C.C
D.D