题目内容
【题目】下列各组物质中为同位素的是
A. 1H与2H B. O2与O3 C. 乙烯与丙烯 D. 异戊烷与新戊烷
【答案】A
【解析】A.1H与2H是质子数相同,中子数不同的同一元素,互称同位素,故A正确;B.O2与O3是氧元素的不同单质,互称同素异形体,故B错误;C.乙烯与丙烯是结构相似,在分子组成上相差1个CH2-原子团,属于同系物,故C错误;D.异戊烷与新戊烷是分子式相同都为C5H12,但结构不同,碳链异构,属于同分异构体,故D错误;故选A。
点晴:本题考查了同位素的判断。根据同位素的概念,质子数相同中子数不同的同一元素互称同位素,同位素是不同的原子,但是属于同一种元素。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案【题目】I.甲醇是一种重要化工原料,又是一种可再生能源,具有开发和应用的广阔前景。
(1)已知:CH3OH(g)=HCHO(g)+H2(g) △H=+84 kJ/mol 2H2(g)+O2(g)=2H2O(g) △H=-484 kJ/mol。工业上常以甲醇为原料制取甲醛,请写出 CH3OH (g)与O2 (g)反应生成HCHO(g)和H2O(g)的热化学方程式:_______________________。
(2)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。该电池负极的电极反应式为________________。
Ⅱ.在2L密闭容器中,800℃时反应2NO(g)+O2 (g)![]() 2NO2 (g)体系中,n(NO)随时间的变化如表:
2NO2 (g)体系中,n(NO)随时间的变化如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)如图所示,表示NO2变化曲线的是_______,用O2表示从0~2 s内该反应的平均速率v=_______。
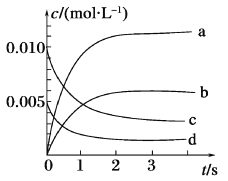
(2)能说明该反应已达到平衡状态的是_______(填序号)。
a.v(NO2) =2V(O2) b.容器内压强保持不变
c.体系颜色不再改变 d.容器内密度保持不变