题目内容
【题目】某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种组成。现进行如下实验:
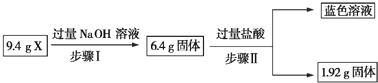
下列有关说法正确的是( )
A. 步骤Ⅰ中质量减少3 g的固体一定是混合物
B. 步骤Ⅱ中质量减少的物质一定是Cu
C. 根据上述步骤Ⅱ可以得出m(Fe2O3)∶m(Cu)=1∶1
D. 根据步骤Ⅰ、Ⅱ可以判断混合物X的成分为Al2O3、Fe2O3、Cu、SiO2
【答案】C
【解析】9.4gX与过量的氢氧化钠溶液反应后得到6.4g不溶物,固体部分溶解,原固体中至少含有Al2O3、SiO2的一种物质;6.4g固体与过量的盐酸反应得到蓝色溶液,蓝色溶液中存在铜离子,发生了反应:Fe2O3+6H+=2Fe3++3H2O、Cu+2Fe3+=2Fe2++Cu2+,说明混合物中一定存在铜和Fe2O3,1.92g固体为铜,则A.Al2O3、SiO2都能够与NaOH溶液反应,所以步骤I中减少的3g固体可能为氧化铝或二氧化硅,不一定为混合物,A错误;B.步骤II中发生了反应:Fe2O3+6H+=2Fe3++3H2O、Cu+2Fe3+=2Fe2++Cu2+,6.4g固体为铜和Fe2O3的混合物,减少的为铜和氧化铁,B错误;C.6.4g变成1.92g,质量减少:6.4g-1.92g=4.48g,减少的质量为Fe2O3和部分Cu,剩余的1.92g为铜,设铜的物质的量为x,根据反应Cu+2Fe3+=2Fe2++Cu2+可知氧化铁的物质的量也为x,则64x+160x=4.48,解得x=0.02mol,氧化铁的质量是0.02mol×160g/mol=3.2g,铜的质量是6.4g-3.2g=3.2g,则m(Fe2O3)∶m(Cu)=1∶1,C正确;D.根据以上分析可知氧化铝和二氧化硅至少含有一种,D错误;答案选C。

 阅读快车系列答案
阅读快车系列答案
