题目内容
16.在容积为2.0L的密闭容器中充入0.60mol X和1.60mol Y,发生反应:aX(g)+3Y(g)?2Z(g)经过10min反应达到平衡状态,Y的浓度为0.2mol/L,Z的物质的量分数为$\frac{4}{7}$计算并回答:
①10分钟内,Z的平均反应速率为0.04mol/(L.min)
②计算a 的值是1
③该条件下反应aX(g)+3Y(g)?2Z(g)的逆反应的平衡常数为0.005
④平衡后容器内的压强为反应前的$\frac{7}{11}$ 倍.
⑤若将体积比为 1:3的X和Y的混合气体,重新通入上述恒容的密闭容器中,在一定的条件下发生反应,达到化学平衡时,混合气体中X的体积分数为 w%;保持温度不变,在原平衡的基础上再次以1:3的比例充入少量X和Y,达到新平衡后混合气体中X的体积分数减小(填“增大”“减小”“不变”).
分析 在容积为2.0L的密闭容器中充入0.60mol X和1.60mol Y,经过10min反应达到平衡状态,Y的浓度为0.2mol/L,平衡时Y为2L×0.2mol/L=0.4,则:
aX(g)+3Y(g)?2Z(g)
起始量(mol):0.6 1.6 0
变化量(mol):0.4a 1.2 0.8
平衡量(mol):0.6-0.4a 0.4 0.8
①根据v=$\frac{△c}{△t}$计算v(Z);
②Z的物质的量分数为$\frac{4}{7}$,则$\frac{0.8}{1.8-0.4a}$=$\frac{4}{7}$,解得a=1;
③该条件下反应aX(g)+3Y(g)?2Z(g)的逆反应的平衡常数K=$\frac{c(X)×{c}^{3}(Y)}{{c}^{2}(Z)}$;
④恒温恒容下,压强之比等于物质的量之比;
⑤保持温度不变,在原平衡的基础上再次以1:3的比例充入少量X和Y,等效为在原平衡的基础上增大压强,平衡正向移动,Z的体积分数增大,由于X、Y起始物质的量之比为1:3,二者又按物质的量1:3反应,故体系中X、Y的体积分数之比为1:3.
解答 解:在容积为2.0L的密闭容器中充入0.60mol X和1.60mol Y,经过10min反应达到平衡状态,Y的浓度为0.2mol/L,平衡时Y为2L×0.2mol/L=0.4,则:
aX(g)+3Y(g)?2Z(g)
起始量(mol):0.6 1.6 0
变化量(mol):0.4a 1.2 0.8
平衡量(mol):0.6-0.4a 0.4 0.8
①v(Z)=$\frac{\frac{0.8mol}{2L}}{10min}$=0.04mol/(L.min),故答案为:0.04mol/(L.min);
②Z的物质的量分数为$\frac{4}{7}$,则$\frac{0.8}{1.8-0.4a}$=$\frac{4}{7}$,解得a=1,故答案为:1;
③该条件下反应aX(g)+3Y(g)?2Z(g)的逆反应的平衡常数K=$\frac{c(X)×{c}^{3}(Y)}{{c}^{2}(Z)}$=$\frac{\frac{0.2}{2}×(\frac{0.4}{2})^{3}}{(\frac{0.8}{2})^{2}}$=0.005,
故答案为:0.005;
④恒温恒容下,压强之比等于物质的量之比,故平衡后容器内的压强为反应前的$\frac{(0.2+0.4+0.8)mol}{(0.6+1.6)mol}$=$\frac{7}{11}$,故答案为:$\frac{7}{11}$;
⑤保持温度不变,在原平衡的基础上再次以1:3的比例充入少量X和Y,等效为在原平衡的基础上增大压强,平衡正向移动,Z的体积分数增大,由于X、Y起始物质的量之比为1:3,二者又按物质的量1:3反应,故体系中X、Y的体积分数之比为1:3,则达到新平衡后混合气体中X的体积分数减小,故答案为:减小.
点评 本题考查化学平衡有关计算,注意三段式解题法在化学平衡计算中应用,⑤中注意对等效平衡的理解,难度中等.

| A. | 采用直接加热绿矾(FeSO4•xH2O)晶体的方法制备无水硫酸亚铁 | |
| B. | 用KMnO4标准溶液滴定H2C2O4溶液时,眼睛时刻关注着锥形瓶内溶液颜色变化 | |
| C. | 在中和热测定实验中,为保证稀盐酸充分反应,将氢氧化钠溶液应分少量多次加入 | |
| D. | 为测定新制氯水pH,用玻璃棒蘸取液体滴在pH试纸上,再对照标准比色卡读数 |
| A. | 呈碱性 | B. | 呈酸性 | C. | 呈中性 | D. | c(OH-)=10c(H+) |
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| n(HI)/mol | 0.180 | 0.164 | 0.152 | 0.144 | 0.140 | 0.140 |
(1)0~2min内H2的平均反应速度为0.002mol/(L•min).达平衡时,HI的转化率是22.2%.
(2)当上述反应达平衡时,降低温度,原化学平衡向逆向移动(填“正向”,“逆向”或“不”),上述正向反应是:吸热反应(选填:放热、吸热),逆反应速率减小(填“增大”、“减小”或“不变”).
(3)480℃时,反应H2(g)+I2(g)?2HI(g)的平衡常数K的值为49.
(4)要增大反应2HI(g)?H2(g)+I2(g)的平衡常数,可采取的措施是D(选填字母).
A.增大HI起始浓度 B.向混合气体中通入I2 C.使用高效催化剂 D.升高温度.
| A. | 卤素单质的沸点按F2、Cl2、Br2、I2的顺序依次增大 | |
| B. | 卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由易变难 | |
| C. | 卤化氢的热稳定性和还原性按HF、HCl、HBr、HI的顺序依次减弱 | |
| D. | 卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深 |
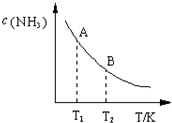 氨在国民经济中占有重要地位.请回答有关氨的下列问题:
氨在国民经济中占有重要地位.请回答有关氨的下列问题:
