��Ŀ����
��Һ������Ũ�ȴ�С�ıȽ�
���Ȼ����Һ�У����й�ϵʽ��ȷ����
A��C(Cl-)��C(NH4+)��C(H+)��C(OH-) B ��C(NH4+)��C(Cl-)��C(H+)��CC(OH-)
������C��C(Cl-)��C(NH4+)��C(H+)��C(OH-) D��C(NH4+)��C(Cl-)��C(H+)��C(OH-)
��0.1 mol/l��NH3��H2O��Һ�У����й�ϵ��ȷ����
��A��C(NH3��H2O)��C(OH-)��C(NH4+)��C(H+) B��C(NH4+)��C(NH3��H2O)��C(OH-)��C(H+)
��C��C(NH3��H2O)��C(NH4+)��C(OH-)��C(H+) D��C(NH3��H2O)��C(NH4+)��C(H+)��C(OH-
�����ʵ�������0.1 mol��CH3COOH��CH3COONa���Ƴ�1L�����Һ����֪����C(CH3COO-)��C(Na+)���Ըû����Һ�������ж���ȷ����( )
������A.C(H+)��C(OH-) B.C(CH3COOH)��C(CH3COO-)��0.2 mol/L
������C.C(CH3COOH)��C(CH3COO-) D.C(CH3COO-)��C(OH-)��0.2 mol/L
A A B

��ϰ��ϵ�д�
�����Ŀ
�ڲ�ͬ�¶��£�ˮ��Һ��c��H+����c��OH-������ͼ��ʾ��ϵ������˵����ȷ���ǣ�������
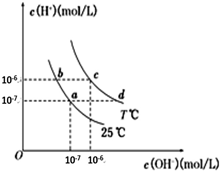

| A��a���Ӧ����Һ��c���Ӧ����ҺpHֵ��С��pH��c����pH��a�� | B��d���Ӧ����Һ�д������ڣ�K+��Ba2+��NO3-��I- | C��25��ʱ��Ka��HF��=3.6��10-4��Ka��CH3COOH��=1.75��10-5��0.1mol/L��NaF��Һ��0.1mol/L ��CH3COOK��Һ��ȣ�c��Na+��-c��F-����c��K+��-c��CH3COO-�� | D����b���Ӧ����Һ��ֻ��NaHA������Һ������Ũ�ȴ�С��c��HA-����c��H2A����c��H+����c��A2-�� |