题目内容
【题目】如图为实验室制备乙炔并进行性质验证的装置(夹持仪器己略去)。
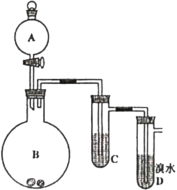
(1)实验室制备乙炔的方程式为___;
(2)仪器A的名称为___,为防止气体生成的速率过快,由A滴入B的试剂为___;
(3)装置C可选用的试剂为___(写出一种即可),其作用为___;
(4)反应开始后,D中的现象为___,所发生反应的反应类型为___;
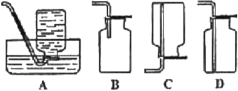
(5)D中验证实验结束后。B中反应仍在继续。此时可撤去装置D,在装置C之后连接收集装置,以下装置中最适合用于收集乙炔的是___。
【答案】CaC2+2H2O→Ca(OH)2+C2H2↑ 分液漏斗 饱和食盐水 NaOH溶液(或CuSO4溶液) 除去气体中的杂质 溴水褪色 加成反应 A
【解析】
碳化钙(CaC2)与水反应生成氢氧化钙[Ca(OH)2]和乙炔,为减缓反应,可用饱和食盐水代替水;得到的乙炔气体中混有H2S等还原性有毒气体,可以用NaOH溶液或硫酸铜溶液来除去;乙炔含有不饱和键,能够与溴水发生加成反应,使溴水褪色;乙炔难溶于水,可以用排水法收集。
(1)碳化钙(CaC2)与水反应生成氢氧化钙[Ca(OH)2]和乙炔,配平即可,方程式为CaC2+2H2O→Ca(OH)2+C2H2↑,故答案为:CaC2+2H2O→Ca(OH)2+C2H2↑;
(2)仪器A为分液漏斗,乙炔与水反应剧烈,为减缓反应,可用饱和食盐水,故答案为:分液漏斗;饱和食盐水;
(3)电石中往往混有CaS等杂质,与水反应会产生H2S等还原性有毒气体,硫化氢能与NaOH溶液或硫酸铜溶液反应,可以用NaOH溶液或硫酸铜溶液除去,故答案为:NaOH溶液(或CuSO4溶液);除去气体中的杂质;
(4)乙炔能够和溴水发生加成反应,方程式为:CH≡CH+2Br2→CHBr2CHBr2,D中的现象为溴水褪色;故答案为:溴水褪色;加成反应;
(5)乙炔难溶于水选择A收集,在装置C之后连接收集装置,最适合用于收集A排水法收集,气体纯度高,故答案为:A。

【题目】某课题组从植物香料中分离出一种罕见的醇(醇A),其结构简式如下。

(1)根据课内所学知识,该醇可发生的反应包括:___(填字母序号)
A.与金属Na反应 B.与CuO反应
C.与浓盐酸反应 D.消去反应
I.该课题组设计了以醇A为原料制备某物质的合成路线。合成反应的第一步。拟使醇A与浓氢溴酸(质量分数47.6%)在90℃下充分反应,制备中间产物B。实验装置如图所示(夹持及加热仪器略去)。

已知:①HBr溶液受热时,HBr能否蒸发受到体系汇总含水量的影响。具体情况如下表。
| <47.6% | 47.6% | >47.6% |
先蒸发的物质 | 水先蒸发,直至比值升至47.6% | HBr与水按该比例一起蒸发、液化沸点124.3℃ | HBr先蒸发,直至比值降至47.6% |
②醇A、中间产物B的沸点均超过200℃。
(2)温度计1拟用于监控反应温度,温度计2拟用于监控实验中离开烧瓶的物质的沸点。两个温度计中,水银球位置错误的是___(填“温度计1”或“温度计2”)其水银球应___;
(3)实验时,冷凝水应从冷凝管的___(填“a口”或“b口”)流入。
II.将温度计位置调节好后,课题组成员依次进行如下操作:
①检验气密性,装入沸石;
②加入18.6g醇A(0.1mol)、17.0g47.6%氢溴酸(含8.1gHBr、0.1mol);
③开始加热,逐渐升温至反应温度。
(4)反应开始后,当温度计2的示数上升至39℃时,冷凝管末端持续有液体流出。反应结束时,共收集到无色液体7.0g。经检测,该液体为纯净物,标记为产物C。取0.7gC在氧气中充分燃烧,共收集到2.2gCO2、0.9gH2O。另取少量C进行质谱试验,结果如图所示。
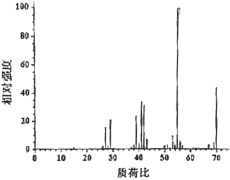
根据上述实验结果,C的分子式为___;
(5)取少量产物C进行核磁共振氢谱试验,共有三个信号峰。三个信号峰的面积之比为3:6:1。综合上述实验结果,C的结构简式为___;
(6)反应结束后,圆底烧瓶内液体分为两层。可用___方法(填实验操作名称)将两液体分离;
(7)后续检验证实,两液体均较纯净,其中所含杂质均可忽略。上层液体质量为10.7g。取下层液体进行核磁共振氢谱实验,共有两个信号峰。峰的面积之比为3:2。综合以上信息,本实验的实际总反应方程式为___。
【题目】高炉炼铁过程中发生反应:![]() Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g) ![]()
![]() Fe(s)+CO2(g),该反应在不同温度下的平衡常数见表。
Fe(s)+CO2(g),该反应在不同温度下的平衡常数见表。
温度T/℃ | 1000 | 1150 | 1300 |
平衡常数K | 4.0 | 3.7 | 3.5 |
下列说法正确的是
A. 增加高炉的高度可以有效降低炼铁尾气中CO的含量
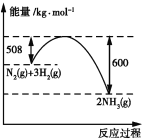
B. 由表中数据可判断该反应:反应物的总能量>生成物的总能量
C. 为了使该反应的K增大,可以在其他条件不变时,增大c(CO)
D. 1000℃下Fe2O3与CO反应,t min达到平衡时c(CO) =2×10-3 mol/L,则用CO表示该反应的平均速率为![]() mol/(L·min)
mol/(L·min)