题目内容
【题目】某化学反应的反应物和产物如下,请按要求回答下列问题![]() :
:
(1)如果该化学方程式中S和![]() 的系数分别是5和1,请配平化学方程式
的系数分别是5和1,请配平化学方程式![]() ,并用单线桥标出电子转移的方向和数目:______。
,并用单线桥标出电子转移的方向和数目:______。
(2)该反应中,发生氧化反应的物质是___,该反应中,发生还原反应的过程是____。
(3)反应中,1mol还原剂________![]() 填“得到”或“失去”
填“得到”或“失去”![]() ________mol电子。
________mol电子。
(4)若在标准状况下,反应产生336ml气体,则转移的电子数为________个。
(5)如果没有对该化学方程式中的某些化学计量数做限定,配平的化学计量数有许多组,原因是________________。
【答案】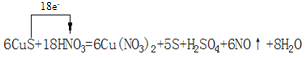
![]()
![]() 失去 3
失去 3 ![]() 该反应的氧化产物有两种,两种氧化产物的化学计量数有许多组。
该反应的氧化产物有两种,两种氧化产物的化学计量数有许多组。
【解析】
(1)已知S和![]() 的系数分别是5和1,S化合价升高,共失18电子,依据电子守恒,可确定NO的化学计量数为6,从而配平方程式。再据单线桥的书写原则,写出表示式;
的系数分别是5和1,S化合价升高,共失18电子,依据电子守恒,可确定NO的化学计量数为6,从而配平方程式。再据单线桥的书写原则,写出表示式;
(2)S元素化合价升高,CuS发生氧化反应,发生还原反应过程为HNO3生成NO;
(3)CuS发生氧化反应,由(1)可知,6CuS失去18电子,则可求出1mol还原剂平均失电子的数目;
(4)标准状况下,反应产生336ml气体,即![]() ,则可求出转移的电子数;
,则可求出转移的电子数;
(5)没有对该化学方程式中的某些化学计量数做限定,配平的化学计量数有许多组,原因是该反应的氧化产物有两种,发生的两个独立反应间没有定量关系。
(1)已知S和![]() 的系数分别是5和1,根据配平原则进行配平,S化合价升高失电子,N化合价降低得电子,反应中转移18电子,则有单线桥法表示为:
的系数分别是5和1,根据配平原则进行配平,S化合价升高失电子,N化合价降低得电子,反应中转移18电子,则有单线桥法表示为: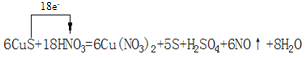 ,故答案为:
,故答案为: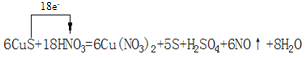 ;
;
(2)S元素化合价升高,CuS发生氧化反应,N化合价降低,![]() 发生还原反应,故答案为:CuS;
发生还原反应,故答案为:CuS;![]() ;
;
(3)CuS发生氧化反应,还原剂为CuS,则1mol还原剂平均失去3mol电子,故答案为:失去;3;
(4)标准状况下,反应产生336ml气体,336mlNO气体的物质的量为0.015mol,则转移的电子数为![]() ,故答案为:
,故答案为:![]() ;
;
(5)没有对该化学方程式中的某些化学计量数做限定,配平的化学计量数有许多组,原因是该反应的氧化产物有两种,两种氧化产物的化学计量数有许多组,故答案为:该反应的氧化产物有两种,两种氧化产物的化学计量数有许多组。

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
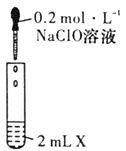
步步高口算题卡系列答案【题目】NaClO是漂白液的有效成分,某研究小组探究NaClO溶液的性质,设计了下列实验:
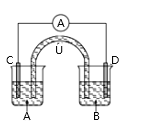
装置图 | 试剂X | 实验现象 | |
|
|
| 产生黄绿色气体 |
|
| 溶液变蓝 | |
|
| 溶液变红 | |
|
| 产生白色沉淀 | |
下列判断不正确的是![]()
![]()
A.实验![]() 中发生的主要反应是
中发生的主要反应是![]()
B.实验![]() 中发生的主要反应是
中发生的主要反应是![]()
C.实验![]() 中该条件下氧化性强弱
中该条件下氧化性强弱![]()
D.实验![]() 中
中![]() 与
与![]() 相互促进水解
相互促进水解
【题目】已知A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。
A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
B元素原子的核外p电子数比s电子数少1 |
C原子的第一至第四电离能分别是:I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
D元素简单离子半径是该周期中最小的 |
E元素是该周期电负性最大的元素 |
F所在族的元素种类是周期表中最多的 |
G在周期表的第十一列 |
(1)已知BA5为离子化合物,写出其电子式__。
(2)B基态原子中能量最高的电子,其电子云在空间有__个方向,原子轨道呈__形。
(3)实验室制备E的单质的离子反应方程式为__。
(4)BE3在常温下是一种淡黄色的液体,其遇水即发生反应可生成一种具有漂白性的物质,写出反应的化学方程式__;该反应说明其中B和E中非金属性较强的是__填元素的符号。
(5)C与D的第一电离能大小为__。D与E的最高价氧化物对应水化物相互反应的离子方程式为__。
(6)G价电子排布图为__,位于__纵行。F元素的电子排布式为__,前四周期中未成对电子数最多的元素在周期表中位置为__(填周期和族)。