题目内容
6.几种短周期元素的原子半径及主要化合价如下表:| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +3、+5、-3 | -2 |
| A. | X、Y元素的金属性 X<Y | |
| B. | 一定条件下,W单质可以将Z单质从其氢化物中置换出来 | |
| C. | Y的最高价氧化物对应的水化物能溶于稀氨水 | |
| D. | 一定条件下,Z单质与W的常见单质直接生成ZW2 |
分析 W化合价为-2价,没有最高正化合价+6价,故W为氧元素;Z元素化合价为+5、+3、-3,Z处于ⅤA族,原子半径与氧元素相差不大,则Z与氧元素处于同一周期,则Z为氮元素;X化合价为+2价,应为周期表第ⅡA族,Y的化合价为+3价,应为周期表第ⅢA族元素,二者原子半径相差较小,可知两者位于同一周期相邻主族,由于X、Y的原子半径与W、Z原子半径相差很小,则X、Y应在第三周期,所以X为镁元素,Y为铝元素.结合元素周期律知识解答该题.
解答 解:A、根据题给数据,X、Y的化合价不同,但原子半径相差较小,则X、Y应在第三周期,所以X为镁元素,Y为铝元素,可知两者位于同一周期相邻主族,故金属性X>Y,故A错误;
B、一定条件下,氧气可以和氨气反应生成水和氮气,故B正确;
C、据此判断可知X是Mg,Y是Al;Y的最高价氧化物的水化物是氢氧化铝,其不溶于氨水,故C错误;
D、根据W、Z分别是O和N,两者的单质直接生成NO,故D错误;
故选:B.
点评 本题考查元素位置结构和性质的关系及应用,题目难度中等,从原子半径的变化和元素的最高正价和最低负价入手寻求突破,正确把握元素化合价、原子半径与元素性质的关系是解答该题的关键.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案
相关题目
17.下列关于元素周期表的说法不正确的是( )
| A. | 元素周期表有7个横行,每一个横行是一周期 | |
| B. | 元素周期表有18个纵行,每一个纵行是一族 | |
| C. | 第ⅡA族元素全部是金属元素 | |
| D. | 第ⅦA族元素全部是非金属元素 |
1.如图为电解CuCl2溶液的装置,其中c、d为石墨电极.则下列有关的判断正确的是( )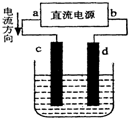

| A. | a为负极、b为正极 | B. | 电解过程中,化学能转化为电能 | ||
| C. | 电解过程中,d电极质量增加 | D. | 电解过程中,C电极发生还原反应 |
11.F2和Xe在一定条件下可生成氧化性极强且极易水解的XeF2、XeF4和XeF6三种化合物.如XeF4与水可发生如下反应:6XeF4+12H2O═2XeO3+4Xe↑+24HF+3O2↑.下列判断中正确的是( )
| A. | XeF2分子中各原子均达到8电子稳定结构 | |
| B. | 上述反应中氧化产物和还原产物的物质的量之比为5:4 | |
| C. | 上述反应中氧化剂和还原剂的物质的量之比为2:1 | |
| D. | XeF4按上述方式水解,每生成4molXe,转移12mol电子 |
18.化合物 是一种除草剂,它含有的官能团为( )
是一种除草剂,它含有的官能团为( )
 是一种除草剂,它含有的官能团为( )
是一种除草剂,它含有的官能团为( )| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
15.下列烷烃的命名正确的是( )
| A. | 2,3-二甲基丁烷 | B. | 3,4-二甲基戊烷 | ||
| C. | 2-甲基-3-乙基丁烷 | D. | 2-乙基己烷 |