��Ŀ����
����Ŀ��[���ʽṹ������]
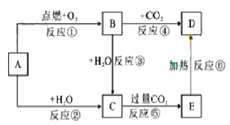
��֪������ͭ��Һ�е��백�������ƣ�H2N��CH2��COONa�����ɵõ������A����ṹ��ͼ1��
��1��CuԪ�ػ�̬ԭ�ӵ���Χ�����Ų�ʽΪ ��
��2��Ԫ��C��N��O�ĵ�һ�������ɴ�С����˳��Ϊ ��
��3�������A��̼ԭ�ӵĹ���ӻ�����Ϊ ��
��4��1mol���������ƣ�H2N��CH2��COONa�����ЦҼ�����ĿΪ ��
��5�����������Ʒֽ����֮һΪ������̼��д��������̼��һ�ֵȵ����壺��д��ѧʽ����
��6����֪������ͭ���տ�������һ�ֺ�ɫ���壬��ṹ��ͼ2����û�����Ļ�ѧʽ�� ��
���𰸡�
��1��3d104s1
��2��N��O��C
��3��sp3��sp2
��4��8mol
��5��N2O����SCN����N3���ȣ�
��6��Cu2O
���������⣺��1��Cu��29��Ԫ�أ���ԭ�Ӻ�����29�����ӣ�3d�ܼ�����10�����ӡ�4s�ܼ�����1�����ӣ�3d��4s�ܼ��ϵ���Ϊ����Χ���ӣ����ݹ���ԭ��֪���̬ԭ����Χ�����Ų�ʽΪ3d104s1��
���Դ��ǣ�3d104s1��
��2��ͬ���ڴ����ң�Ԫ�صĵ�һ�����ܳ��������ƣ���NԪ��ԭ�ӵ�2p�ܼ����ڰ����ȶ�״̬�������ϵͣ���һ�����ܸ���ͬ�������ڵ�Ԫ�أ�����C��N��O����Ԫ�صĵ�һ����������С���������˳����N��O��C��
���Դ��ǣ�N��O��C��
��3�������A������һ��̼��C=O��̼���ӻ���ʽΪsp2�ӻ�����һ��̼��Χ���ǵ�����̼���ӻ���ʽΪsp3�ӻ���
���Դ��ǣ�sp3��sp2��
��4�����۵���Ϊ�Ҽ�������˫����һ���ǦҼ�һ���Ǧм���H2N��CH2��COONa�к���8���Ҽ�������1mol�����������к��ЦҼ�����ĿΪ8mol��
���Դ��ǣ�8mol��
��5��һ��������̼������ԭ�Ӹ���Ϊ3�����۵�����Ϊ16��ԭ�Ӹ�����ȡ��۵�������ȵ���Ϊ�ȵ����壬��CO2�ĵȵ�����Ϊ��N2O����SCN����N3���ȣ���
���Դ��ǣ�N2O����SCN����N3���ȣ���
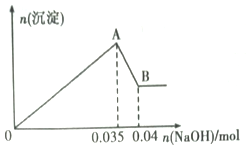
��6�����þ�̯��֪���û�������Oԭ�Ӹ���=1+8�� ![]() =2��Cuԭ�Ӹ���=4��ͭԭ�Ӻ���ԭ�Ӹ���֮��=4��2=2��1�������仯ѧʽΪ��Cu2O��
=2��Cuԭ�Ӹ���=4��ͭԭ�Ӻ���ԭ�Ӹ���֮��=4��2=2��1�������仯ѧʽΪ��Cu2O��
���Դ��ǣ�Cu2O��

 Сѧ�������Ծ�ϵ�д�
Сѧ�������Ծ�ϵ�д�