题目内容
 如图,某同学将KClO3、浓盐酸、镁粉装进试管中,塞好胶塞,片刻后在管外点燃镁条,产生耀眼的白光,立即发现胶塞剧烈冲出.该同学的实验目的是
如图,某同学将KClO3、浓盐酸、镁粉装进试管中,塞好胶塞,片刻后在管外点燃镁条,产生耀眼的白光,立即发现胶塞剧烈冲出.该同学的实验目的是
- A.制取氢气并检验其纯度
- B.制取氯气并检验其纯度
- C.验证氯酸钾的氧化性
- D.验证光对氢气和氯气反应的作用
D
分析:KClO3、浓盐酸反应生成氯气,浓盐酸、镁粉反应生成氢气,而片刻后在管外点燃镁条,产生耀眼的白光,立即发现胶塞剧烈冲出,是因试管外的光照导致氢气、氯气反应,以此来解答.
解答:KClO3、浓盐酸反应生成氯气,浓盐酸、镁粉反应生成氢气,而片刻后在管外点燃镁条,产生耀眼的白光,立即发现胶塞剧烈冲出,是因试管外的光照导致氢气、氯气反应,则该实验的实验目的为验证光对氢气和氯气反应的作用,而该实验中没有进行气体的纯度的检验及验证氯酸钾的氧化性,
故选D.
点评:本题以性质实验设计考查实验目的,注意实验操作中“片刻后在管外点燃镁条”为解答的关键,题目难度中等.
分析:KClO3、浓盐酸反应生成氯气,浓盐酸、镁粉反应生成氢气,而片刻后在管外点燃镁条,产生耀眼的白光,立即发现胶塞剧烈冲出,是因试管外的光照导致氢气、氯气反应,以此来解答.
解答:KClO3、浓盐酸反应生成氯气,浓盐酸、镁粉反应生成氢气,而片刻后在管外点燃镁条,产生耀眼的白光,立即发现胶塞剧烈冲出,是因试管外的光照导致氢气、氯气反应,则该实验的实验目的为验证光对氢气和氯气反应的作用,而该实验中没有进行气体的纯度的检验及验证氯酸钾的氧化性,
故选D.
点评:本题以性质实验设计考查实验目的,注意实验操作中“片刻后在管外点燃镁条”为解答的关键,题目难度中等.

练习册系列答案
相关题目
氯化铝融盐电解法是以氯化铝为原料,以碱金属或碱土金属氯化物(含少量MgCl2、KCl、CaCl2)为电解质进行电解制取铝的方法。
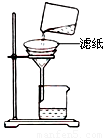
(1)氯化铝融盐电解法需要先制纯氧化铝。以铝土矿(主要成分为Al2O3,含有少量Fe2O3、SiO2等杂质)为原料通过以下途径提纯氧化铝:
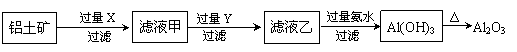
 |
①依次写出X、Y的成分 , 。
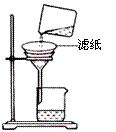
②如右图所示在实验室中进行过滤,
操作中的两处错误分别是 ;
。
(2)制备无水氯化铝的反应为:2Al2O3+6Cl2![]() 4AlCl3+3O2
4AlCl3+3O2
③为促进该反应的进行,实际生产中需加入焦炭,其原理是 。
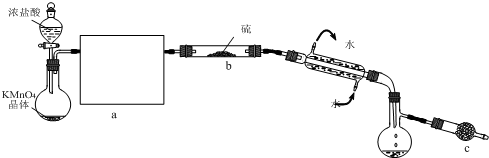
④加入焦炭后的化学反应可表示为Al2O3+C+Cl2![]() AlCl3+X↑,为确定气体X是否是混合气体,某同学将X依次通过灼热的氧化铜和澄清的石灰水,再根据现象判断。该操作是否正确?(填正确、不正确或无法判断) ,请说明理由 。
AlCl3+X↑,为确定气体X是否是混合气体,某同学将X依次通过灼热的氧化铜和澄清的石灰水,再根据现象判断。该操作是否正确?(填正确、不正确或无法判断) ,请说明理由 。
(3)现在工业上通常用电解熔融氧化铝方式制取铝,理论上生产1吨铝消耗的氧化铝的质量 (填“大于”、“小于”、“等于”)氯化铝质量。
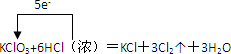
 本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应和答题区域内作答.若两题都做,则按A题评分.
本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应和答题区域内作答.若两题都做,则按A题评分.
 4AlCl3+3O2
4AlCl3+3O2
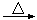 AlCl3+X↑,为确定气体X是否是混合气体,某同学将X依次通过灼热的氧化铜和澄清的石灰水,再根据现象判断。该操作是否正确?(填正确、不正确或无法判断) ,请说明理由
。
AlCl3+X↑,为确定气体X是否是混合气体,某同学将X依次通过灼热的氧化铜和澄清的石灰水,再根据现象判断。该操作是否正确?(填正确、不正确或无法判断) ,请说明理由
。