题目内容
600 ℃时,在一密闭容器中,将二氧化硫和氧气混合发生反应:2SO2(g)+O2(g)①反应从0 min开始,到第一次平衡时,二氧化硫的转化率为50% ②反应进行到10 min至15 min的曲线变化一定是升高了温度 ③反应进行至20 min时,曲线发生变化是因为通入了氧气 ④在15—20 min和25—30 min内时反应处于平衡状态 ⑤反应进行到10 min至15 min的曲线变化可能是加入催化剂或缩小了容器的体积
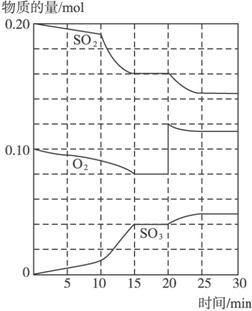
A.①②③ B.①④⑤ C.②③④ D.③④⑤
D
解析:①SO2转化率为![]() ×100%=20%;②也可为增大压强,使用效率更好的催化剂;③从图中看出n(O2)由0.08 mol增至0.12 mol而其他物质不变;④两段时间内各物质的量均不变。
×100%=20%;②也可为增大压强,使用效率更好的催化剂;③从图中看出n(O2)由0.08 mol增至0.12 mol而其他物质不变;④两段时间内各物质的量均不变。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2 (g)?2SO3(g) (△H<0)
在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2 (g)?2SO3(g) (△H<0)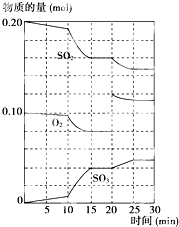 在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g)?2SO3(g)△H<0
在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g)?2SO3(g)△H<0 (2004?上海)在一定条件下,二氧化硫和氧气发生如下反应:
(2004?上海)在一定条件下,二氧化硫和氧气发生如下反应: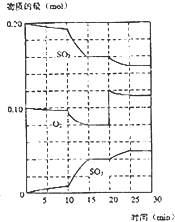 在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g)?2SO3(g)△H<0
在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g)?2SO3(g)△H<0 2SO3(g)△H<0
2SO3(g)△H<0
