题目内容
【题目】下列说法正确的是
A. 25℃时,pH均为1的盐酸和醋酸加水稀释1000倍,所得溶液的pH:醋酸>盐酸
B. 等体积、等物质的量浓度的NH4HSO4和KOH溶液混合:c(K+)=c(SO42-)>c(NH4+)>c(OH-)>c(H+)
C. 25℃时,pH=12的氨水和pH=2的盐酸等体积混合,所得溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
D. 浓度均为0.1 molL-1的HClO溶液和NaClO溶液等体积混合,溶液中有下列关系:c(HC1O)+2c(H+)=c(C1O-)+2c(OH-)
【答案】D
【解析】A. 醋酸是弱电解质,HCl是强电解质,25℃时,pH均为1的盐酸和醋酸加水稀释1000倍,稀释促进醋酸电离,所得溶液的pH:醋酸<盐酸,故A错误;B. 等体积、等物质的量浓度的NH4HSO4和KOH溶液混合,中和反应恰好完全进行,形成等浓度的K2SO4和(NH4)2SO4的混合溶液, ![]() +H2O
+H2O![]() NH3 H2O+H+,所以c(K+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-),故B错误;C. 25℃时,pH=12的氨水和pH=2的盐酸等体积混合,一水合氨难电离,物质的量浓度大于盐酸,中和反应剩余大量一水合氨,NH3·H2O
NH3 H2O+H+,所以c(K+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-),故B错误;C. 25℃时,pH=12的氨水和pH=2的盐酸等体积混合,一水合氨难电离,物质的量浓度大于盐酸,中和反应剩余大量一水合氨,NH3·H2O![]()
![]() +
+ ![]() -,所得溶液中: c(NH4+)> c(Cl-)>c(OH-)>c(H+),故C错误;D. 浓度均为0.1 molL-1的HClO溶液和NaClO溶液等体积混合,HClO
-,所得溶液中: c(NH4+)> c(Cl-)>c(OH-)>c(H+),故C错误;D. 浓度均为0.1 molL-1的HClO溶液和NaClO溶液等体积混合,HClO![]() ClO-+ H+,ClO-+ H2O
ClO-+ H+,ClO-+ H2O![]() HClO+OH-,溶液中电荷守恒:c(Na+)+c(H+)=c(C1O-)+c(OH-),元素守恒:2c(Na+)=c(C1O-)+c(HC1O),两个表达式消去c(Na+)得c(HC1O)+2c(H+)=c(C1O-)+2c(OH-),故D正确。故选D。
HClO+OH-,溶液中电荷守恒:c(Na+)+c(H+)=c(C1O-)+c(OH-),元素守恒:2c(Na+)=c(C1O-)+c(HC1O),两个表达式消去c(Na+)得c(HC1O)+2c(H+)=c(C1O-)+2c(OH-),故D正确。故选D。

【题目】能源、环境与生产生活和社会发展密切相关.
(1)一定温度下,在两个容积均为2L的密闭容器中,分别发生反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H=﹣49.0kJmol﹣1 . 相关数据如表:
容器 | 甲 | 乙 |
反应物投入量 | 1mol CO2(g)和3mol H2(g) | 1mol CH3OH (g)和 |
平衡时c(CH3OH) | c1 | c2 |
平衡时能量变化 | 放出29.4kJ | 吸收a kJ |
①下列情况能说明该反应一定达到平衡状态的是(填字母).
a.v(CO2)消耗=v(CH3OH)生成
b.气体的密度不再随时间改变
c.CO2和CH3OH的浓度之比不再随时间改变
d.气体的平均相对分子质量不再随时间改变
②其他条件不变,达到平衡后,下列不能提高H2转化率的操作是(填字母).
a.降低温度b.充入更多的H2c.移除甲醇d.增大容器体积
③c1c2(填“>”“<”或“=”),a= .
④该温度下反应的平衡常数K=;若甲中反应10s时达到平衡,则0~10s内甲中的平均反应速率v(H2)= .
(2)已知反应:2NO2(红棕色)N2O4(无色)△H<0.将一定量的NO2充入注射器后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小).下列说法正确的是(填字母). 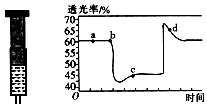
A.b点的操作是拉伸注射器
B.d点:v正<v逆
C.c点与a点相比,c(NO2)增大,c(N2O4)减小
D.若不忽略体系温度变化,且没有能量损失,则Tb>Tc .