题目内容
【题目】A、B、C、D 为原子序数依次增大的四种元素,A2和 B+具有相同的电子构型;C、D 为同周期元素,C 核外电子总数是最外层电子数的 3 倍;D 元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是_____(填元素符号),其中 C 原子的外围电子排布图为_____.
(2)单质 A 有两种同素异形体,其中沸点高的是_________(填分子式),原因是_____;A 和 B 的氢化 物所含的化学键类型分别为_____和_____.
(3)C 和 D 反应可生成组成比为 1:3 的化合物 E,E 的立体构型为_____,中心原子的杂化轨 道类型为_____.
(4)化合物 D2A 的立体构型为_____,中心原子的价层电子对数为_____,单质 D与湿润的 Na2CO3 反应可制备 D2A,其化学方程式为_____。
【答案】 O ![]() O3 O3 相对原子质量较大,范德华力较大 共价键 离子键 三角锥形 sp3 V 形 4 2Cl2+2Na2CO3+H2O=Cl2O+2NaHCO3+2NaCl(或 2Cl2+Na2CO3=Cl2O+CO2+2NaCl)
O3 O3 相对原子质量较大,范德华力较大 共价键 离子键 三角锥形 sp3 V 形 4 2Cl2+2Na2CO3+H2O=Cl2O+2NaHCO3+2NaCl(或 2Cl2+Na2CO3=Cl2O+CO2+2NaCl)
【解析】C核外电子总数是最外层电子数的3倍,应为P元素,C、D为同周期元素,则应为第三周期元素,D元素最外层有一个未成对电子,应为Cl元素,A2-和B+具有相同的电子构型,结合原子序数关系可知A为O元素,B为Na元素。
(1)同周期自左而右电负性增大,Cl元素氧化物中氧元素表现负价,四种元素电负性最大的为O元素;C为P元素,原子核外电子数为15,根据能量最低原理原理,核外电子排布图为:![]() ,故答案为:O;
,故答案为:O;![]() ;
;
(2)A为O元素,有O2、O3两种同素异形体,二者对应的晶体都为分子晶体,因O3相对原子质量较大,则范德华力较大,沸点较高,A 和 B 的氢化物分别为水和氢化钠,化学键分别为共价键和离子键,故答案为:O3;O3相对原子质量较大,范德华力较大;共价键;离子键;
(3)C和D生成组成比为1:3的化合物E为PCl3,P原子形成3个P-Cl键,含有1对孤对电子,立体构型为为三角锥形,杂化轨道数目为3,P原子采取sp3杂化,故答案为:三角锥形;sp3;
(4)化合物D2A为Cl2O,O为中心原子,形成2个σ键,孤电子对数为![]() =2,则中心原子的价层电子对数为4,立体构型为V形,氯气与湿润的Na2CO3反应得到Cl2O,由电子转移守恒可知,先得到HCl生成,HCl再与碳酸钠反应,反应的方程式为:2Cl2+2Na2CO3+H2O=Cl2O+2NaHCO3+2NaCl(或2Cl2+Na2CO3=Cl2O+CO2+2NaCl),故答案为:V形;4;2Cl2+2Na2CO3+H2O=Cl2O+2NaHCO3+2NaCl(或2Cl2+Na2CO3=Cl2O+CO2+2NaCl)。
=2,则中心原子的价层电子对数为4,立体构型为V形,氯气与湿润的Na2CO3反应得到Cl2O,由电子转移守恒可知,先得到HCl生成,HCl再与碳酸钠反应,反应的方程式为:2Cl2+2Na2CO3+H2O=Cl2O+2NaHCO3+2NaCl(或2Cl2+Na2CO3=Cl2O+CO2+2NaCl),故答案为:V形;4;2Cl2+2Na2CO3+H2O=Cl2O+2NaHCO3+2NaCl(或2Cl2+Na2CO3=Cl2O+CO2+2NaCl)。

 快乐5加2金卷系列答案
快乐5加2金卷系列答案【题目】应用 VSEPR 理论判断下表中分子或离子的立体构型。
分子 | 中心原子上弧电子对数 | 中心原子结合的杂化类型 | 分子或离子的立体构型 |
NH2 | _______________ | _______________ | _______________ |
BF3 | _______________ | _______________ | _______________ |
H3O+ | _______________ | _______________ | _______________ |
【题目】工业上可用铬铁矿(主要成分可表示为FeO·Cr2O3,还含有Al2O3、MgCO3、SiO2等杂质)为原料制备重铬酸钾晶体和绿矾的流程如下:
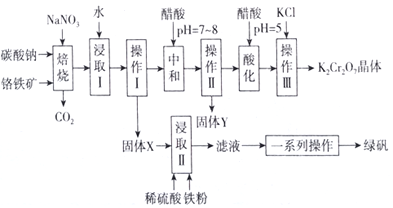
已知:Ⅰ.常见离子沉淀的pH范围
Fe3+ | Al3+ | Mg2+ | SiO32- | AlO2- | |
开始沉淀 | 1.9 | 4.2 | 8.1 | 9.5 | 10.2 |
沉淀完全 | 3.2 | 5.3 | 9.4 | 8.0 | 8.5 |
Ⅱ.焙烧过程中主要发生反应:2FeO·Cr2O3+4Na2CO3+7NaNO3=4Na2Cr2O4+Fe2O3+4CO2↑+7NaNO2。
(1)绿矾的化学式为________。
(2)焙烧后的混合物中除含有Na2Cr2O4、NaNO2和过量的Na2CO3、NaNO3外,还含有NaAlO2和Na2SiO3等物质,则焙烧过程中NaAlO2的化学方程式为___________________________。
(3)固体Y的主要成分为________(填写化学式)。
(4)酸化过程中用醋酸调节pH=5的目的为________________________;若pH调节的过低,NO2-可被氧化为NO3-,其离子方程式为_________________________________。
(5)调节pH=5后,加入KCl控制一定条件,可析出K2Cr2O7晶体,说明溶解度的大小:K2Cr2O7________Na2Cr2O7(填“大于”或“小于”)。
(6)流程中的一系列操作为____________________________________。