题目内容
【题目】某化学兴趣小组在实验室探究氨的有关性质,设计了下图所示实验,A处是气体发生装置,A中所用的实验药品从下列物质中选取.
①碳酸钠 ②碳酸氢钠 ③碳酸氢铵 ④氯化铵 ⑤熟石灰 ⑥氢氧化钠

按上图连接好各仪器,现将C处的铂丝网加热至红热,再将A处产生的气体通过B装置片刻后撤去C处酒精灯,部分实验的现象如下:铂丝继续保持红热状态,D中的铜片慢慢溶解,回答下列问题:
(1)若A中制取气体时只用了一种药品,则该药品是 (填物质序号)
(2)B装置的作用为
(3)D中铜片发生反应的离子方程式为 ,为了使Cu片溶解的速率加快,可向D处的溶液中加入下列少量物质中的 (填下列各项序号)
A.Na2CO3 B.AgNO3 C.H2SO4 D.FeSO4
(4)图E中持续通人氧气的作用为 。
(5)有人认为他们设计的这套实验装置还存在明显的不足,对其不足之处以及应如何改进,谈谈你的意见: 。
【答案】(1)③(2)吸收二氧化碳和水蒸气并产生氧气
(3)3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O B C
(4)使有害气体吸收更完全
(5)D装置的液体易倒流入玻璃管C中,使玻璃管破裂,在C装置与D装置之间连接一防倒吸装置。
【解析】
试题分析:根据题给装置图及C、D中反应现象知,本实验为探究氨的催化氧化及硝酸与铜的反应,装置A的作用为生成氨气,装置B的作用为反应提供氧气,装置E和F为尾气处理装置。(1)根据上述分析知,A中生成的气体中含有氨气和过氧化钠反应生成氧气的气体二氧化碳、水蒸气;A中制取气体时只用了一种药品,分析选项可知一种试剂生成氨气和二氧化碳的试剂选择碳酸氢铵,答案为:③;(2)B装置是利用过氧化钠吸收碳酸氢铵分解生成的二氧化碳和水蒸气生成氧气,答案为:吸收二氧化碳和水蒸气并产生氧气;(3)D中反应为铜片溶于稀硝酸生成硝酸铜、一氧化氮和水,离子方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;使Cu片溶解的速率加快,可以利用原电池原理及增大离子浓度的方法;A、Na2CO3消耗硝酸,硝酸浓度减小,反应速率减慢,错误;B、AgNO3和铜反应生成银,铜和银在稀硝酸溶液中析出原电池加快反应速率,正确;C、H2SO4会增大氢离子浓度加快铜与稀硝酸的反应速率,正确;D、FeSO4会消耗硝酸不能加快铜的反应速率,错误;选BC;(4)图E中持续通入氧气的作用是使生成的一氧化氮气体全部转化为硝酸而被完全吸收,答案为:使有害气体吸收更完全;(5)D装置中的液体易发生倒吸到C装置,需要在CD之间加一个防倒吸的装置,答案为:D装置的液体易倒流如玻璃管C中,使玻璃管破裂,在C与D装置之间连接一个防止倒吸的装置。

【题目】结合下表回答下列问题(均为常温下的数据):
酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
CH3COOH | 1.8×10-5 | H2CO3 | K1=4.4×10-7 K2=4.7×10-11 | H2C2O4 | K1=5.4×10-2 K2=5.4×10-5 | H2S | K1=1.3×10-7 K2=7.1×10-15 |
HClO | 3×10-8 |
请回答下列问题:
Ⅰ.(1)同浓度的CH3COO-、HCO、CO![]() 、HC2O4- 、ClO-、S2-结合H+的能力最弱的____________。
、HC2O4- 、ClO-、S2-结合H+的能力最弱的____________。
(2)常温下0.1 mol·L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的
是________(填序号)。
A.c(H+) B.c(H+)/c(CH3COOH)
C.c(H+)·c(OH-) D. ![]()
若该溶液升高温度,上述4种表达式的数据增大的是_________________。
(3)体积为10 mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中pH 变化如图所示,则稀释后,醋酸溶液中由水电离出来的c(H+)_______(填“大于”、“等于”或“小于”)HX 溶液中由水电离出来的c(H+)。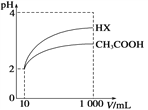
Ⅱ.(1)下列化学方程式可能正确的是______________。
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
(2)写出过量CO2通入Na2S溶液中的离子方程式______________________________________。
(3)将过量的氯气通入到少量的碳酸钠溶液中_______________________________________。
