题目内容
【题目】侯德榜制碱法生产流程为:
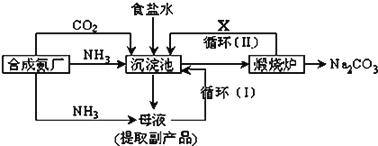
![]() 沉淀池中反应的化学方程式:________________________________;
沉淀池中反应的化学方程式:________________________________;
![]() 检验产品碳酸钠中是否含有氯化钠的操作方法为:___________________________
检验产品碳酸钠中是否含有氯化钠的操作方法为:___________________________
![]() 上述流程中物质X的分子式为 ______
上述流程中物质X的分子式为 ______
【答案】![]() 用硝酸酸化的硝酸银,观察到若产生白色沉淀则说明有氯化钠存在,若不生成沉淀,则无氯化钠
用硝酸酸化的硝酸银,观察到若产生白色沉淀则说明有氯化钠存在,若不生成沉淀,则无氯化钠 ![]()
【解析】
(1)饱和食盐水中通入氨气和二氧化碳析出碳酸氢钠晶体;
(2)检验产品碳酸钠中是否含有氯化钠即检验是否含氯离子,可以用硝酸酸化的硝酸银;
(3)循环Ⅱ是利用碳酸氢钠分解生成的二氧化碳通入沉淀池循环使用。
(1)氨气、二氧化碳、水和氯化钠发生反应生成碳酸氢钠和氯化铵,反应方程式为![]() ,故答案为:
,故答案为:![]() ;
;
(2)检验产品碳酸钠中是否含有氯化钠即检验是否含氯离子,可以用硝酸酸化的硝酸银,观察到若产生白色沉淀则说明有氯化钠存在,若不生成沉淀,则无氯化钠;故答案为:用硝酸酸化的硝酸银,观察到若产生白色沉淀则说明有氯化钠存在,若不生成沉淀,则无氯化钠;
(3)循环Ⅰ是将未反应的氯化钠返回沉淀池中,煅烧碳酸氢钠时生成二氧化碳、二氧化碳能循环利用,所以X是![]() ,故答案为:
,故答案为:![]() 。
。

 优学名师名题系列答案
优学名师名题系列答案【题目】在相同条件下,做H2O2分解对比实验时,回答下面问题:
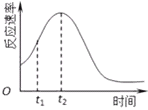
(1)其中①加人MnO2催化,②不加MnO2催化。下图是反应放出O2的体积随时间的变化关系示意图,其中正确的是_______________
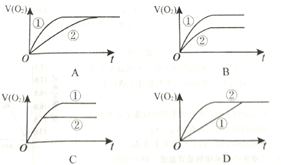
(2)将质量相同但聚集状态不同的MnO2分别加入到5 mL 5%的双氧水中,并用带火星的木条测试。测定结果如下:
催化剂(MnO2) | 操作情况 | 观察结果 | 反应完成所需的时间 |
粉末状 | 混合不振荡 | 剧烈反应,带火星的木条复燃 | 3.5分钟 |
块状 | 反应较慢,火星红亮但木条不复燃 | 30分钟 |
①写出H2O2的电子式______________发生的化学反应方程式_______________________。
②实验结果说明催化剂作用的大小与____________有关。