题目内容
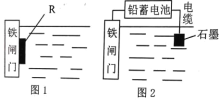
【题目】如图,A池用石墨电极电解NaOH溶液,B池精炼粗铜,一段时间后停止通电,A池中D极产生具有氧化性的气体在标准状况下为2.24L。下列说法正确的是( )

A.A池为电解池,B池为原电池
B.D、E两极都发生氧化反应
C.E极应为粗铜板材料
D.B池中E极质量增加12.8g
【答案】D
【解析】
已知A池用石墨电极电解NaOH溶液,B池精炼粗铜,一段时间后停止通电,A池中D极产生具有氧化性的气体在标准状况下为2.24L,电解NaOH溶液,在阳极生成氧气具有氧化性,阴极生成氢气,则可判断D极为电解池A的阳极,C为阴极;则E电极为阴极,F电极为阳极;则可推得A池电解氢氧化钠溶液,D电极生成氧气,C电极生成氢气;B池精炼铜,阳极F为粗铜,E电极为精铜,据此解答。
已知A池用石墨电极电解NaOH溶液,B池精炼粗铜,一段时间后停止通电,A池中D极产生具有氧化性的气体在标准状况下为2.24L,电解NaOH溶液,在阳极生成氧气具有氧化性,阴极生成氢气,则可判断D极为电解池A的阳极,C为阴极;则E电极为阴极,F电极为阳极;则可推得A池电解氢氧化钠溶液,D电极生成氧气,C电极生成氢气;B池精炼铜,阳极F为粗铜,E电极为精铜,
A. 有外接电源,A、B都为电解池,A项错误;
B. 电解池中阳极上发生氧化反应,所以应为D、F电极上发生氧化反应,C、E电极上发生还原反应,B项错误;
C. 由以上分析可知,B池精炼铜,阳极F为粗铜,E电极为精铜;C项错误;
D. B池中E极为电解池阴极,电极反应Cu2++2e=Cu,质量增加为铜,A池中D电极生成氧气,电极反应:4OH4e=2H2O+O2↑,生成氧气物质的量为0.1mol,失电子物质的量为0.4mol,根据串联电解池中转移电子数相等,可知E极得电子为0.4mol,则生成铜0.2mol,质量为12.8g,D项正确;
答案选D。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案