��Ŀ����
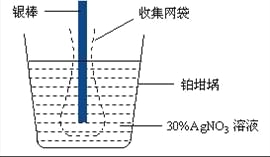
����Ŀ��(9��)����ͼװ��ʵ�飬A��B���ձ��ֱ�ʢ��200 g10%NaOH������CuSO4��Һ��ͨ��һ��ʱ���c������Cu�������ֲ��A������Һ����������4.5 g(������ˮ������)��
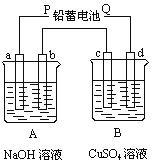
��ش��������⣺
��1����ԴP��Ϊ����������ֱ�д��b����c���Ϸ����ĵ缫��Ӧ ʽ�� ��
��2��c������������ͭ������Ϊ g
��3����װ������Ǧ��������Դ����֪Ǧ���طŵ�ʱ�������·�Ӧ��
������Pb��SO42 ����PbSO4��2e��
������PbO2��4H����SO42 ����2e��=PbSO4��2H2O
������a���Ƶ�����0.050 mol����ʱ��������ĵ�H2SO4�����ʵ����������� ��mol
���𰸡��Ÿ� 4OH��-4e����2H2O��O2�� Cu2����2e��=Cu ��16 g ��0.10 mol
��������
������c������Cu������˵��cΪ���ص�������dΪ��������PΪ������bΪ���NaOH��Һ������������ӦΪ4OH��-4e��=2H2O��O2����cΪ�������ͭ��Һ��������������ӦΪCu2����2e��=Cu��
���ձ�A�з������ܷ�ӦʽΪ2H2O![]() 2H2����O2����A������Һ����������4.5 g��ӦΪ���ʱ����ˮ��������n(H2O)=
2H2����O2����A������Һ����������4.5 g��ӦΪ���ʱ����ˮ��������n(H2O)=![]() =0.25 mol��ת�Ƶ���Ϊ0.5 mol��c������������ͭ�����ʵ���Ϊ0.25 mol��������Ϊ0.25 mol��64 g/mol=16 g��
=0.25 mol��ת�Ƶ���Ϊ0.5 mol��c������������ͭ�����ʵ���Ϊ0.25 mol��������Ϊ0.25 mol��64 g/mol=16 g��
��a���Ƶ����������ʵ���Ϊ0.050 mol����ת��������Ϊ0.10 mol������Ǧ�����ܷ�ӦʽΪPb��PbO2��2H2SO4=2PbSO4��2H2O�����������ĵ�H2SO4�����ʵ���������0.10 mol��

 ��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д� �����������Ż�ѧϰϵ�д�
�����������Ż�ѧϰϵ�д�