题目内容
【题目】现有a mol/L 的NaX和b mol/L的NaY两种盐溶液。下列说法正确的是
A.若a=b且c(X-)= c(Y-)+ c(HY),则HX为强酸
B.若a=b且pH(NaX)>pH(NaY),则c(X-)+ c(OH-)> c(Y-)+ c(OH-)
C.若a>b且c(X-)= c(Y-),则酸性HX>HY
D.若两溶液等体积混合,则c(Na+)=(a+b) mol/L(忽略混合过程中的体积变化)
【答案】A
【解析】
试题分析:A.若a=b,且c(X-)=c(Y-)+c(HY),说明HX完全电离,所以能说明HX为强酸,故A 正确;B.若a=b且pH(NaX)>pH(NaY),根据电荷守恒得c(Na+)+c(H+)=c(X-)+c(OH-),c(Na+)+c(H+)=c(Y-)+c(OH-),根据物料守恒得两种溶液中c(Na+)相等,根据溶液的PH知,X-的水解程度大于Y-,所以NaX中氢离子浓度小于NaY,所以c(X-)+c(OH-)<c(Y-)+c(OH-),故B错误;C.若a>b且c(X-)=c(Y-),说明X- 的水解程度大于Y-,酸根离子水解程度越大,其相应酸的酸性越弱,则酸性HX<HY,故C错误;D.若两溶液等体积混合,钠离子不水解,但溶液体积增大一倍,所以则c(Na+)=![]() mol/L,故D错误;故选A。
mol/L,故D错误;故选A。

【题目】下表为4种常见溶液中溶质的质量分数和物质的量浓度:
溶 质 | HCl | NaOH | CH3COOH | HNO3 |
溶质的质量分数/% | 36.5 | 40 | 60 | 63 |
物质的量浓度/mol·L-1 | 11.8 | 14.3 | 10.6 | 13.8 |
这4种溶液中密度最小的是( )
A.HCl B.NaOH C.CH3COOH D.HNO3
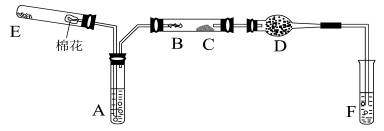
【题目】苯甲酸广泛应用于制药和化工行业。某同学尝试用甲苯的氧化反应制备苯甲酸。
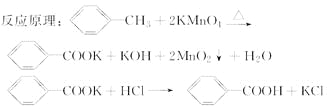
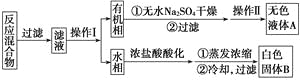
实验方法:一定量的甲苯和KMnO4溶液在100 ℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。
已知:苯甲酸分子量122,熔点122.4 ℃,在25 ℃和95 ℃时溶解度分别为0.3 g和6.9 g;纯净固体有机物一般都有固定熔点。
(1)操作Ⅰ为________,操作Ⅱ为________。
(2)无色液体A是________,定性检验A的试剂是________,现象是________。
(3)测定白色固体B的熔点,发现其在115 ℃开始熔化,达到130 ℃时仍有少量不熔。该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。请在完成表中内容。
序号 | 实验方案 | 实验现象 | 结果 |
① | 将白色固体B加入水中,加热溶解,________ | 得到白色晶体和无色滤液 | |
② | 取少量滤液于试管中,________ | 生成白色沉淀 | 滤液含Cl- |
③ | 干燥白色晶体,________ | ________ | 白色晶体是苯甲酸 |
(4)纯度测定:称取1.220 g产品,配成100 mL苯甲酸溶液,移取25.00 mL溶液,滴定,消耗KOH的物质的量为2.40×10-3mol,产品中苯甲酸质量分数的计算结果为________(保留2位有效数字)。