题目内容
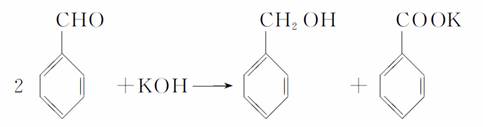
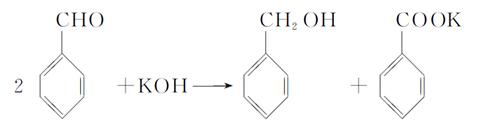
实验室中用苯甲醛制备苯甲醇和苯甲酸,已知反应原理: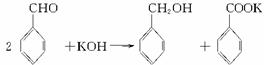
苯甲醛易被空气氧化;苯甲醇的沸点为
试完成下列问题:
(1)混合苯甲醛、氢氧化钾和水应选用的仪器是________________。
A.带胶塞的锥形瓶 B.玻璃棒和玻璃片
C.烧杯 D.容量瓶
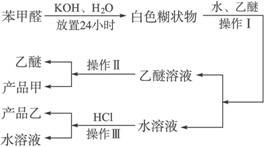
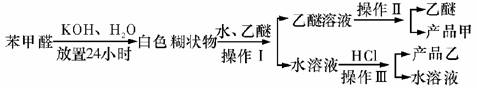
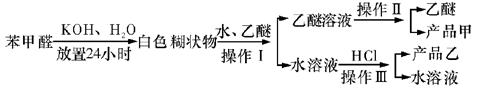
(2)操作Ⅰ的名称是_____________,乙醚溶液中的主要成分是_____________。
(3)操作Ⅱ的名称是_____________。
(4)操作Ⅲ的名称是_____________,产品乙是_____________。
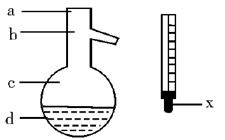
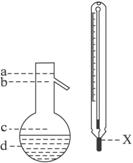
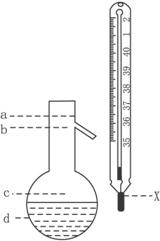
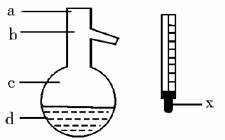
(5)在使用图示仪器的操作中,温度计水银球的上沿X的放置位置为_____________(填图示a、b、c、d)。该操作中,除图中两仪器外,还需使用的仪器有酒精灯、带附件的铁架台、橡胶塞、各种玻璃导管、橡胶管及_____________等必要仪器。分离产品的适宜温度是_____________。
(1)A (2)分液 苯甲醇 (3)蒸馏 (4)过滤苯甲酸 (5)b石棉网、冷凝管、接收器、尾锥管
解析:依题给信息,白色糊状物应为苯甲醇和苯甲酸钾的混合物。加水、乙醚,因为二者互不相溶,溶液会分层,再依据相似相溶原理,水层中应溶有苯甲酸钾,乙醚层应溶有苯甲醇。分液就可以把水层、乙醚层分开。乙醚与苯甲醇沸点差很大,可用蒸馏法进行分离。苯甲酸钾水溶液加HCl后会生成苯甲酸,苯甲酸在水中溶解度很小,过滤可得苯甲酸。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
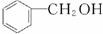
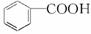
 (填序号)。
(填序号)。 。
。