题目内容
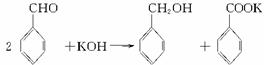
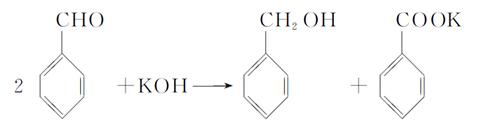
实验室中用苯甲醛制备苯甲醇和苯甲酸,已知反应原理:
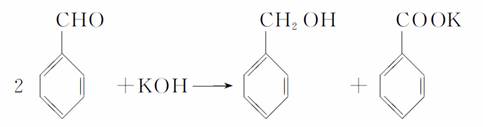
苯甲醛易被空气氧化;苯甲醇的沸点为205.3℃;苯甲酸的熔点121.7℃,沸点249℃,溶解度0.34g(常温);乙醚的沸点34.8℃,难溶于水。
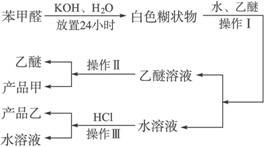
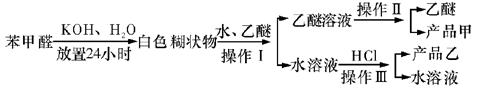
制备苯甲醇和苯甲酸的主要过程如下:
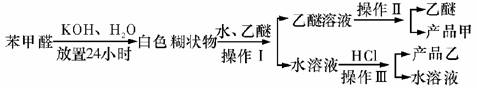
(1)混合苯甲醛、氢氧化钾和水应选用的仪器是 (填序号)。
A.带胶塞的锥形瓶 B.烧杯
C.容量瓶
(2)操作I的名称是 。
(3)操作II的名称是 ,产品甲的成分是 。
(4)操作III的名称是 ,产品乙是 。
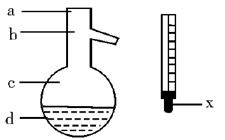
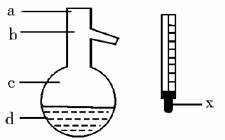
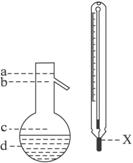
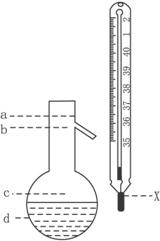
(5)在使用下图所示的仪器的操作中,温度计水银球x的放置位置为 (填图标a、b、c、d)。控制蒸气的温度为 。
(1)A (2)分液 (3)蒸馏 苯甲醇
(4)过滤 苯甲酸 (5)b 34.8℃
【解析】(1)因苯甲醛易被空气氧化。
(2)据相似相溶原理知,苯甲醇溶于乙醚之中,苯甲酸钾(盐)溶于水之中,二者应出现分层现象。
(3)因乙醚和苯甲醇沸点相差较大,易于控制温度获得不同的馏分。
(4)利用了强酸能制取弱酸的原理:C6H5—COOK+HCl →C6H5COOH↓+KCl,过滤即得苯甲酸。
(5)选用b的理由是,为了测量蒸气的温度。

练习册系列答案
相关题目
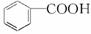
 (填序号)。
(填序号)。 。
。