题目内容
油画置于空气中,天长日久就会生成黑色的PbS从而使油画的色彩变暗,若用H2O2来“清洗”,则可使PbS转变为白色的PbSO4,从而使油画“复原”。?
(1)请写出“清洗”反应的化学方程式,此反应体现了H2O2的什么性质?????
(2)若有0.100 mol的PbS参与反应,则在此反应中发生转移的电子的物质的量为_________mol。?
(1)请写出“清洗”反应的化学方程式,此反应体现了H2O2的什么性质?????
(2)若有0.100 mol的PbS参与反应,则在此反应中发生转移的电子的物质的量为_________mol。?
(1)PbS+4H2O2====PbSO4+4H2O;体现了H2O2的氧化性。
(2)0.800
(2)0.800
写出题设条件下发生反应的化学方程式是解决(1)(2)两问的关键。
(1)从题意来看反应物是明确的,应是PbS和H2O2;H2O2具有强氧化性,使PbS中-2价的S变为PbSO4中+6价的S,H2O2中-1价的O得电子后变为-2价,所以生成物应是PbSO4和H2O。于是得方程式为:PbS+4H2O2====PbSO4+4H2O。
(2)由(1)得PbS与转移电子的关系:
PbS~8e-
则转移电子的物质的量为:n(e-)=8n(PbS)="0.800" mol。
(1)从题意来看反应物是明确的,应是PbS和H2O2;H2O2具有强氧化性,使PbS中-2价的S变为PbSO4中+6价的S,H2O2中-1价的O得电子后变为-2价,所以生成物应是PbSO4和H2O。于是得方程式为:PbS+4H2O2====PbSO4+4H2O。
(2)由(1)得PbS与转移电子的关系:
PbS~8e-
则转移电子的物质的量为:n(e-)=8n(PbS)="0.800" mol。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 2Na2S+Na2SO3+3H2O。当有1mol硫发生反应时,被还原的硫有( )
2Na2S+Na2SO3+3H2O。当有1mol硫发生反应时,被还原的硫有( )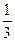 mol
mol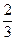 mol
mol