题目内容
(10分)
某实验需要100 mL、0.1 mol/L的Na2CO3溶液,现通过如下操作配制:
①把称量好的固体Na2CO3放入小烧杯中,加适量蒸馏水溶解。为加快溶解可以使用 (填仪器名称)搅拌
②把①所得溶液冷却到室温后,小心转入 (填仪器名称)
③继续加蒸馏水至液面至刻度线1~2cm处,改用 (填仪器名称)小心滴加蒸馏水至溶液凹液面最低点与刻度线相切
④用少量蒸馏水洗涤玻璃棒和烧杯2~3次,每次洗涤的溶液都小心转入容量瓶,并轻轻摇匀
⑤将容量瓶塞紧,充分摇匀。
(1)操作步骤正确的顺序是 (填序号)。
(2)若所配溶液的密度为1.06 g/mL,则该溶液的质量分数为 。
(3)若取出20 mL配好Na2CO3的溶液,加蒸馏水稀释成c(Na+) ="0.01" mol/L的溶液,则稀释后溶液的体积为 mL
(4)在配制100 mL、0.1 mol/L的Na2CO3溶液时,下列操作中的 会导致结果偏低(请用
序号填写)
a.将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
b.定容时俯视刻度线
c.定容时仰视刻度线
d.干净的容量瓶未经干燥就用于配制溶液
某实验需要100 mL、0.1 mol/L的Na2CO3溶液,现通过如下操作配制:
①把称量好的固体Na2CO3放入小烧杯中,加适量蒸馏水溶解。为加快溶解可以使用 (填仪器名称)搅拌
②把①所得溶液冷却到室温后,小心转入 (填仪器名称)
③继续加蒸馏水至液面至刻度线1~2cm处,改用 (填仪器名称)小心滴加蒸馏水至溶液凹液面最低点与刻度线相切
④用少量蒸馏水洗涤玻璃棒和烧杯2~3次,每次洗涤的溶液都小心转入容量瓶,并轻轻摇匀
⑤将容量瓶塞紧,充分摇匀。
(1)操作步骤正确的顺序是 (填序号)。
(2)若所配溶液的密度为1.06 g/mL,则该溶液的质量分数为 。
(3)若取出20 mL配好Na2CO3的溶液,加蒸馏水稀释成c(Na+) ="0.01" mol/L的溶液,则稀释后溶液的体积为 mL
(4)在配制100 mL、0.1 mol/L的Na2CO3溶液时,下列操作中的 会导致结果偏低(请用
序号填写)
a.将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
b.定容时俯视刻度线
c.定容时仰视刻度线
d.干净的容量瓶未经干燥就用于配制溶液
玻璃棒;100毫升容量瓶;胶头滴管;①②④③⑤;1%;400;ac
试题分析:加快溶解的正确操作是用玻璃棒搅拌;配制100ml溶液时就需要用100ml容量瓶;定容时需要用胶头滴管。
(1)根据配制的原理及实验要求可知,正确的操作顺序是①②④③⑤。
(2)根据
 可知,该溶液的质量分数为
可知,该溶液的质量分数为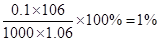 。
。(3)稀释前钠离子的浓度是0.2mol/L,而稀释后钠离子的浓度是0.01mol/L,所以稀释后溶液的体积是
 。
。(4)根据c=n/V可知,将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外,则溶质减少,浓度偏小;定容时俯视刻度线,则溶液的体积减小,所以浓度偏高;反之定容时仰视刻度线,浓度偏低;干净的容量瓶未经干燥就用于配制溶液,不会影响实验结果,答案选ac。
点评:配制一定物质的量浓度溶液的实验是中学化学中一个重要的定量实验,实验过程中引起溶液浓度存在误差的因素有很多。从大的方面讲,一是由实验过程中的不规范操作引起的;二是由仪器或药品等系统原因引起的。由于引起误差的原因复杂,所以误差分析就成为高考化学实验中的一个难点。
在高考命题时,有关误差分析的内容既可以以选择题的形式进行考查,也可以以填空题的形式进行考查,既可以考查判断误差导致的结果,也可以考查引起误差的可能原因。

练习册系列答案
相关题目
