��Ŀ����
����Ŀ����84����Һ����������Һ��Ӧ������ȡ��������Ӧԭ��Ϊ��NaClO + NaCl + H2SO4 ![]() Na2SO4 + Cl2��+ H2O�� Ϊ̽�����������ʣ�ijͬѧ���ô�ԭ���������������������ʾ��ʵ��װ�ã�
Na2SO4 + Cl2��+ H2O�� Ϊ̽�����������ʣ�ijͬѧ���ô�ԭ���������������������ʾ��ʵ��װ�ã�
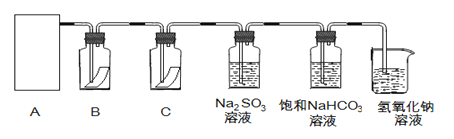
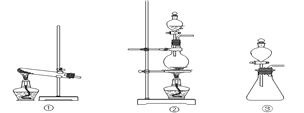
��1���Ӣ١��ڡ���װ����ѡ����ʵ�������װ�ã�A����___________ (��д���)��
��2��װ��B��C�����ηŵ��Ǹ���ĺ�ɫ������ʪ��ĺ�ɫ������ʵ������и�ͬѧ����װ��B�еIJ���Ҳ��ɫ����ԭ�������__________��˵����װ�ô������Ե�ȱ�ݣ�����������ĸĽ��ķ��� _______________________________��
��3��Ϊ����֤�����������ԣ�������ͨ��Na2SO3��Һ�У�Ȼ����鷴Ӧ����Һ���Ƿ���SO42-��д��������Na2SO3��Һ��Ӧ�����ӷ���ʽ ________________�����鷴Ӧ����Һ�к���SO42-�ķ�����ȡ������Ӧ����Һ���Թ��У��ȼ���������_____������������Ȼ���ټ�������____��Һ�а�ɫ�������ɣ�˵������SO42-��
��4������ͨ�뱥��NaHCO3��Һ�ܲ�����ɫ���壬��֪����:����>̼��>�����ᣬ��ʵ��֤��������ˮ��Ӧ���������к��� ________________ ������ᡱ�����ᡱ����
���𰸡� �� �����������к���ˮ�����ᷴӦ���ɴ����� ��װ��A��B֮������ʢ��Ũ�����ϴ��ƿ�������װ�ã� Cl2+SO32-+H2O=SO42-+2Cl-+2H+ ϡ���ᣨ��HCl��Һ�� BaCl2(������������) ����
����������1����NaClO+NaCl+H2SO4![]() Na2SO4+Cl2��+H2O��֪����Ӧ��Һ��μӣ���Ҫ���ȣ�����ѡװ�âڣ���2��װ��B�и������ɫ������ɫ��˵�������п��ܻ���������ˮ������������ˮ��Ӧ���ɴ������Ư�ף����Ӧ����A��B֮������ʢ��ŨH2SO4��ϴ��ƿ����ȥCl2�е�ˮ��������������������ų��������ӵĸ��ţ���˼��鷴Ӧ����Һ�к���SO42���ķ����ǣ�ȡ������Ӧ����Һ���Թ��У��ȼ���������ϡ����������������Ȼ���ټ�������BaCl2��Һ�а�ɫ�������ɣ�˵������SO42-����3��������������������Ϊ�����ƣ���������ԭΪCl-����Ӧ���ӷ���ʽΪCl2+SO32-+H2O��SO42-+2Cl-+2H+����4������ͨ��ˮ��Һ�ᷴӦ��������ʹ����ᣬ�������̼������ᣬ����ͨ�뱥��NaHCO3��Һ�ܲ�����ɫ���壬֤��������ˮ��Ӧ���������к������ᡣ
Na2SO4+Cl2��+H2O��֪����Ӧ��Һ��μӣ���Ҫ���ȣ�����ѡװ�âڣ���2��װ��B�и������ɫ������ɫ��˵�������п��ܻ���������ˮ������������ˮ��Ӧ���ɴ������Ư�ף����Ӧ����A��B֮������ʢ��ŨH2SO4��ϴ��ƿ����ȥCl2�е�ˮ��������������������ų��������ӵĸ��ţ���˼��鷴Ӧ����Һ�к���SO42���ķ����ǣ�ȡ������Ӧ����Һ���Թ��У��ȼ���������ϡ����������������Ȼ���ټ�������BaCl2��Һ�а�ɫ�������ɣ�˵������SO42-����3��������������������Ϊ�����ƣ���������ԭΪCl-����Ӧ���ӷ���ʽΪCl2+SO32-+H2O��SO42-+2Cl-+2H+����4������ͨ��ˮ��Һ�ᷴӦ��������ʹ����ᣬ�������̼������ᣬ����ͨ�뱥��NaHCO3��Һ�ܲ�����ɫ���壬֤��������ˮ��Ӧ���������к������ᡣ

����Ŀ����������(NOCl,�۵�:-64.5 ��,�е�:-5.5 ��)��һ�ֻ�ɫ����,��ˮ��ˮ�⡣�����ںϳ���������ý�����м���ȡ�ʵ���ҿ���������һ�������ڳ��³�ѹ�ºϳɡ�
��1�������ͬѧ���Ʊ�ԭ����NO��Cl2,�Ʊ�װ������ͼ��ʾ:

Ϊ�Ʊ��������������,�±���ȱ�ٵ�ҩƷ��:
װ�â� | װ�â� | ||
��ƿ�� | ��Һ©���� | ||
�Ʊ�����Cl2 | MnO2 | ��___ | ��___ |
�Ʊ�����NO | Cu | ��___ | ��___ |
��2������ͬѧ���ü����Ƶõ�NO��Cl2�Ʊ�NOCl,װ����ͼ��ʾ:

��װ������˳��Ϊa��________(�������������ҷ���,��Сд��ĸ��ʾ)��
��װ�â��������ɽ�һ������NO��Cl2��,��һ��������____________��
��װ�â���������____________��
��װ�â�������β��ʱ,NOCl������Ӧ�Ļ�ѧ����ʽΪ________________��
��3������ͬѧ��������,�����ˮ��Ũ������Ũ����Ļ��ᣬһ�������¸û���������������Ⱥ������� �÷�Ӧ�Ļ�ѧ����ʽΪ__________________��



