��Ŀ����
����Ŀ��������Դ�����þ��й���ǰ����
��1����ͼ�ǴӺ�ˮ����ȡþ�ļ����̣�

��ҵ�ϳ����ڳ���Mg2+���Լ�A��______�����������ƣ���Mg��OH��2ת��ΪMgCl2�����ӷ���ʽ��______��
��2���������и�����I����ʽ���ڵĵ�Ԫ�ء�ʵ������ȡI2��;��������ʾ��
�ɺ���![]() ������
������![]() ��Һ
��Һ![]()
![]()
![]() I2
I2
�����պ������ҽ�ʱ���õ���Ҫ����������______��
�����ữ����Һ�мӹ���������Һ��д���÷�Ӧ�����ӷ���ʽ______��
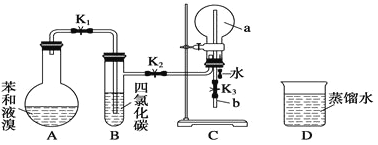
�۷�Ӧ��������CCl4����ȡ����������ȡ����Һ�ķ����ӵ�ˮ����ȡ�⣬��Ҫ����������ͼ��
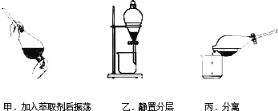
�ס��ҡ���3��ʵ������У�����ȷ����______����ס������ҡ���������
���𰸡� ʯ����������� Mg��OH��2+2H+=Mg2++2H2O ���� 2H++2I��+H2O2�TI2+2H2O ��
��������(1)��ҵ�ϳ���ʯ����������Ƴ���þ���ӣ� ������þ�����ᷴӦ�����Ȼ�þ��ˮ�����ӷ���ʽΪ��Mg��OH��2+2H+=Mg2++2H2O��(2) �����չ���ʱ���õ���Ҫ����Ϊ������ �� ���������Ӻ��������������Ϊ����������������ת��Ϊ���ʵ⣬���ӷ���ʽΪ��2H++2I��+H2O2�TI2+2H2O���������÷ֲ�ٳֺ�����������ʱ�����²�Һ����ϲ�Һ�壬���ͼ��������