题目内容
【题目】铁是地壳中含量仅次于铝的金属元素.铁及其化合物在生活、生产中有广泛应用.请回答下列问题:
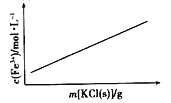
(1)磁铁矿是工业上冶炼铁的原料之一,其原理是![]() ,若有
,若有![]() 参加反应,转移电子的物质的量是 ______ mol.
参加反应,转移电子的物质的量是 ______ mol.
(2)高铁酸钾![]() 是一种既能杀菌、消毒,又能絮凝净水的水处理剂.工业制备高铁酸钾的方法为在KOH浓溶液中加入NaClO和
是一种既能杀菌、消毒,又能絮凝净水的水处理剂.工业制备高铁酸钾的方法为在KOH浓溶液中加入NaClO和![]() ,并不断搅拌,其发生的反应的离子方程式
,并不断搅拌,其发生的反应的离子方程式![]() ______
______
(3)某课外活动小组将下图所示装置按一定顺序连接,在实验室里制取一定量的FeCl3(所通气体过量并充分反应)已知FeCl3会吸水潮解.
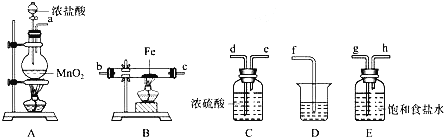
请回答下列问题:
①![]() 中发生反应的化学方程式为 ______ .
中发生反应的化学方程式为 ______ .
②各装置的正确连接顺序为![]() 填写装置代号A
填写装置代号A![]() ______
______ ![]() ______
______ ![]() ______
______ ![]() ______
______![]() D。
D。![]() 其中C用了两次
其中C用了两次![]()
③装置E的作用是 ______ ,写出装置D中反应的离子方程式 ______ .
④反应开始后,B中硬质玻璃管内的现象为 ______ ;FeCl3常作净水剂,原理是 ______ ![]() 用离子方程式表示
用离子方程式表示![]()
【答案】8 ![]() MnO2+4HCl(浓)
MnO2+4HCl(浓)![]() MnCl2+Cl2+2H2O E C B C 吸收氯气中的氯化氢
MnCl2+Cl2+2H2O E C B C 吸收氯气中的氯化氢 ![]() 产生棕色的烟
产生棕色的烟 ![]()
![]() 胶体
胶体![]()
【解析】
(1)若有1molFe3O4参加反应,由反应可知4molCO作还原剂,利用C元素的化合价变化计算转移电子;
(2)KOH浓溶液中加入NaClO和Fe(OH)3,生成K2FeO4,Fe元素的化合价升高,则Cl元素的化合价降低,结合电子、电荷守恒分析;
(3)由制备实验装置可知,A中发生4HCl(浓)+MnO2![]() MnCl2+Cl2↑+2H2O,然后利用E除去HCl,利用C干燥氯气,在B中发生Fe与氯气的反应生成氯化铁,连接C可防止氯化铁水解,最后利用D进行尾气处理,以此来解答。
MnCl2+Cl2↑+2H2O,然后利用E除去HCl,利用C干燥氯气,在B中发生Fe与氯气的反应生成氯化铁,连接C可防止氯化铁水解,最后利用D进行尾气处理,以此来解答。
(1)1molFe304参加反应,Fe原子得电子,而C原子失去电子,4molCO作还原剂,则转移的电子为4mol×(4-2)=8mol,故答案为:8;
(2)KOH浓溶液中加入NaClO和Fe(OH)3,生成K2FeO4,Fe元素的化合价升高,则Cl元素的化合价降低,由电子、电荷守恒可知,离子反应为2Fe(OH)3+3ClO-+4OH-═2FeO42-+3Cl-+5H2O,故答案为:2FeO42-+3Cl-+5H2O;
(3)①A中发生反应的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
②制备氯气中含有氯化氢和水蒸气,除去氯化氢气体用饱和食盐水,除去水蒸气用浓硫酸,应先除氯化氢,后干燥,还要防止氯化铁水解,最后吸收尾气中未反应的氯气,防止污染空气,所以装置顺序为A→E→C→B→C→D,故答案为:E;C;B;C;
③E的作用为吸收氯气中的氯化氢,D中的离子反应为2OH-+Cl2=Cl-+ClO-+H2O,故答案为:吸收氯气中的氯化氢;2OH-+Cl2=Cl-+ClO-+H2O;
④反应开始后,B中硬质玻璃管内的现象为产生棕色的烟,FeCl3常作净水剂,原理是Fe3++3H2OFe(OH)3+3H+,
故答案为:产生棕色的烟;Fe3++3H2OFe(OH)3(胶体)+3H+。

【题目】Ⅰ.(化学反应原理)
25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
请回答下列问题:
(1)CH3COOH的电离平衡常数表达式__。
(2)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为__。
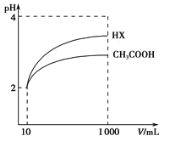
(3)体积均为l00mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数___(填“大于”、“小于”或“等于”)醋酸的电离平衡常数。
Ⅱ.(化学与生活)
防治环境污染,改善生态环境已成为全球共识。
(1)燃煤气化有助于减少PM2.5,写出焦炭与水蒸气反应的化学方程式___。
(2)采用焚烧处理垃圾进行发电已在江苏投入使用。下列是生活中的常见垃圾:
A.废纸 B.废电池 C.易拉罐 D.玻璃瓶 E.塑料制品
在焚烧处理前,除废电池外,还有___(填字母)应剔除并回收,随意丢弃电池造成的主要危害是___。