��Ŀ����
����Ŀ����ʽ̼����[Nix(OH)y(CO3)z��nH2O]��һ����ɫ��ĩ���������������մ���ɫ����300 ������ʱ�ֽ����� 3 ����������Ϊȷ������ɣ�ijͬѧ��ʵ���ҽ������йص�̽���� ��ش�����������

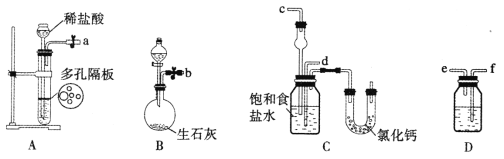
(1)װ�� E ��������������_____��
(2)�ס�����װ�ÿɷֱ�ѡȡ����װ��_____��_____(����ĸ��װ�ÿ��ظ�ѡȡ)��

(3) ��װ��ʵ�����������װ������������ȡһ�����ļ�ʽ̼������Ʒ������Ӳ�ʲ������ڣ� ����Ӳ�ʲ���������װ�� C ��_____(��ʵ������)ʱ��ֹͣ���������� K������ͨ��һ��ʱ�������������ʵ�顣
(4)װ�� A ��������______________________________________________________________________��
(5)ʵ��ǰ�����±���ʾ���ݣ�
װ�� B ����Ʒ����/g | װ�� C ����/g | װ�� D ����/g | |
ʵ��ǰ | 3.77 | 132.00 | 41.00 |
ʵ��� | 2.25 | 133.08 | 41.44 |
��֪��ʽ̼������ Ni ���ϼ�Ϊ��2 ������ü�ʽ̼�����Ļ�ѧʽΪ_______________________________��
���𰸡����θ���� c c ���������ݲ��� ���տ����е� CO2 ��ˮ��������ֹ����ʵ���� Ni3(OH)4CO3��4H2O
��������
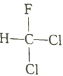
(1) ���������Ľṹ�жϣ�
(2)���ɵ�CO2Ӧ���ü�ʯ�����գ����Լס�����װ�þ�ѡ���ʯ����
(3)��Ӧ����CO2���ɣ����Ե�װ��C�в��������ݲ���ʱ��ֹͣ������
(4)�������Ϸ�����֪װ��A�����������տ����е�CO2��ˮ������
(5)���ݱ������ݿ�֪���ɵ�ˮ��1.08 g�����ɵ�CO2��0.44 g����Ϸ�Ӧ�Ƴ����ʵĻ�ѧʽ��
(1) ���������Ľṹ��֪��װ�� E �����������������θ���ܣ�
(2)����װ���к��п�������Ҫ�����ɵ�������ȫ�ž���������Ҫ���ÿ�����װ���еĿ����Լ����ɵ������ž��������ڿ����к���ˮ������CO2������ͨ��ǰ��Ҫ���ü�ʯ�Ҿ�����������Ӧ�����ɵ�ˮ������Ũ�������գ����ɵ�CO2Ӧ���ü�ʯ�����գ����Լס�����װ�þ�ѡ���ʯ�ң���Ϊc��c��
(3)��Ӧ����CO2���ɣ����Ե�װ��C�в��������ݲ���ʱ��ֹͣ������
(4)�������Ϸ�����֪װ��A�����������տ����е�CO2��ˮ������
(5)���ݱ������ݿ�֪���ɵ�ˮ��1.08 g�����ʵ�����0.06 mol�����ɵ�CO2��0.44 g�����ʵ�����0.01 mol�� ������ٵ�������3.77g 2.25g=1.52 g=0.44g+1.08g����˵����Ӧ�е���������NiO�� H2O��CO2������NiO 2.25g�����ʵ�����0.03 mol����x:z=3: 1�����ݵ���غ��֪2x=y+2z�����y=4z������ѧʽ��Ni3(OH)4CO3n(H2O)���������ɵĽᾧˮ�����ʵ�����0.06 mol-0.02 mol= 0.04 mol������������ʵĻ�ѧʽΪNi3(OH)4CO3��4H2O��

����Ŀ������ʵ�������Ӧ����������ʵ����
|
|
|
|
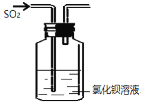
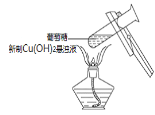
A��������������ͨ���Ȼ�����Һ�У�������ɫ���������ᱵ | B��������Cu(OH)2����Һ�м��������������ǣ����ȣ�����ש��ɫ���� | C����������Ͷ�뵽��ˮ�Ҵ��У��Ʊ��������ݲ��� | D����ʢˮ���ձ��м����Ȼ��ƹ��壬С���ݻ��������� |
A. AB. BC. C...D. D