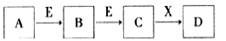题目内容
(13分).巳知 A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物。其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1 mol 丁分子中不同原子的数目比为1 :2,且含有18 mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用。各物质间的转化关系如下图所示(某些条件巳略去)。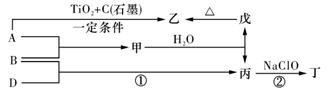
请回答:(1)单质B的组成元素在周期表中的位置是_________。
(2)戊的化学式为________。戊与强碱反应的离子方程式:________________
(3)丙中所包含的化学键类型有________ (填字母序号)。
a.离子键 b.极性共价键 c.非极性共价键
(4)反应①的化学方程式为________________________。
(5)反应②中,0.5mol NaClO参加反应时,转移1 mol电子,其化学方程式为_________
(6)—定条件下,A与TiO2、C(石墨)反应只生成乙和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分。巳知,该反应生成1 mol乙时放出536 kJ热量,其热化学方程式为_______________________
(1)第二周期,第ⅤA族;(2)Al(OH)3,Al(OH)3+OH-=AlO2-+2H2O;(3)b;
(4)N2+H2 2NH3;(5)2NH3+NaClO=N2H4+NaCl+H2O;
2NH3;(5)2NH3+NaClO=N2H4+NaCl+H2O;
(6)4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) ΔH=-1072KJ/mol
解析试题分析:根据题意可知:A是Al; B是N2;C是H2;甲是AlN;乙是Al2O3;丙的NH3;丁是N2H4;戊是Al(OH)3。(1)单质B的组成元素在周期表中的位置是第二周期,第ⅤA族;(2)戊的化学式为Al(OH)3,戊与强碱反应的离子方程式是:Al(OH)3+OH-=AlO2-+2H2O;(3)在丙NH3中所包含的化学键类型有极性共价键,所以选项是b;(4)反应①的化学方程式为N2+H2 2NH3;(5)反应②中,0.5mol NaClO参加反应时,转移1 mol电子,其化学方程式为2NH3+NaClO=N2H4+NaCl+H2O;(6)—定条件下,A与TiO2、C(石墨)反应只生成乙和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分。巳知,该反应生成1 mol乙时放出536 kJ热量,其热化学方程式为4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) ΔH=-1072KJ/mol.
2NH3;(5)反应②中,0.5mol NaClO参加反应时,转移1 mol电子,其化学方程式为2NH3+NaClO=N2H4+NaCl+H2O;(6)—定条件下,A与TiO2、C(石墨)反应只生成乙和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分。巳知,该反应生成1 mol乙时放出536 kJ热量,其热化学方程式为4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) ΔH=-1072KJ/mol.
考点:考查元素及化合物的推断的知识。主要包括元素的位置、物质的化学式的书写、化学方程式、离子方程式、热化学方程式的书写、分子内的化学键的类型的知识。

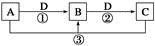
今有甲、乙、丙、丁、戊5种物质,在一定条件下,它们能按下图方式进行转化: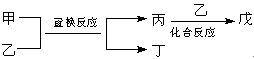
其推断正确的是
| 选项 | 甲 | 乙 | 丙 | 丁 | 戊 |
| A | NH3 | O2 | NO | H2O | NO2 |
| B | Mg | CO2 | C | MgO | CO |
| C | C | H2O | CO | H2 | HCOOH |
| D | FeBr2 | Cl2 | FeCl2 | Br2 | FeCl3 |
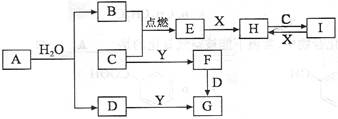
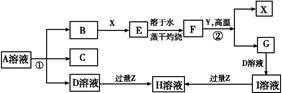
已知X为一种常见酸的浓溶液,能使蔗糖粉末变黑。A与X反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是( )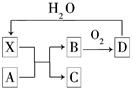
| A.X使蔗糖变黑的现象主要体现了X的强氧化性 |
| B.若A为铁,则足量A与X在室温下即可完全反应 |
| C.若A为碳单质,则将C通入少量的澄清石灰水中,一定可看到白色沉淀 |
| D.工业上,B转化为D的反应条件为高温、常压、使用催化剂 |