题目内容
(1)在3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O反应中,
用双线桥标出该反应电子转移的方向和数目

(2)双线桥标出反应KClO3+6HCl=KCl+3Cl2↑+3H2O电子转移的方向和数目
 .
.
HNO3
HNO3
是氧化剂;Cu
Cu
是还原剂;Cu
Cu
元素被氧化;N
N
元素被还原;Cu(NO3)2
Cu(NO3)2
是氧化产物;NO
NO
是还原产物,被还原的HNO3与参加反应的HNO3物质的量之比是1:4
1:4
.用双线桥标出该反应电子转移的方向和数目


(2)双线桥标出反应KClO3+6HCl=KCl+3Cl2↑+3H2O电子转移的方向和数目


分析:(1)在3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O反应中,Cu元素化合价升高,被氧化,为还原剂,N元素化合价降低,被还原,HNO3为氧化剂,反应中硝酸既表现为氧化性又表现酸性;
(2)反应中KClO3+6HCl=KCl+3Cl2↑+3H2O中,只有Cl元素化合价发生变化,当有3mol Cl2生成时,转移5mol电子.
(2)反应中KClO3+6HCl=KCl+3Cl2↑+3H2O中,只有Cl元素化合价发生变化,当有3mol Cl2生成时,转移5mol电子.
解答:解:(1)在3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O反应中,Cu元素化合价升高,被氧化,为还原剂,N元素化合价降低,被还原,HNO3为氧化剂,Cu(NO3)2是氧化产物,NO是还原产物,反应中硝酸既表现为氧化性又表现酸性,当有8mol HNO3参加反应时,生成2molNO,被还原的HNO3与参加反应的HNO3物质的量之比是1:4,用双线桥标出该反应电子转移的方向和数目为 ,
,
故答案为:HNO3;Cu;Cu;N;Cu(NO3)2;NO;1:4; ;
;
(2)反应中KClO3+6HCl=KCl+3Cl2↑+3H2O中,只有Cl元素化合价发生变化,当有3mol Cl2生成时,转移5mol电子,则电子转移的方向和数目为 ,故答案为:
,故答案为: .
.
 ,
,故答案为:HNO3;Cu;Cu;N;Cu(NO3)2;NO;1:4;
 ;
;(2)反应中KClO3+6HCl=KCl+3Cl2↑+3H2O中,只有Cl元素化合价发生变化,当有3mol Cl2生成时,转移5mol电子,则电子转移的方向和数目为
 ,故答案为:
,故答案为: .
.点评:本题考查氧化还原反应,侧重于学生的分析能力的考查,为高考常见题型和高频考点,注意从元素化合价的角度分析,能用双线桥标出电子转移的方向和数目,难度不大.

练习册系列答案
相关题目
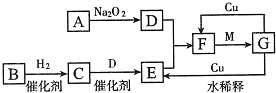 如图表示由短周期元素组成的一些物质之间的转化关系(某些反应产物已略去).各方框表示有关的一种反应物或生成物(某些物质已经略去),其中A、B、D在常温下均为无色无刺激性气味的气体,C是使湿润的红色石蕊试纸变蓝的气体,M是最常见的无色液体.
如图表示由短周期元素组成的一些物质之间的转化关系(某些反应产物已略去).各方框表示有关的一种反应物或生成物(某些物质已经略去),其中A、B、D在常温下均为无色无刺激性气味的气体,C是使湿润的红色石蕊试纸变蓝的气体,M是最常见的无色液体.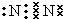
 科研小组为探究氮的化合物性质,按如图连接好装置,进行实验.将C处Pt丝加热至红热,再将A试管中物质加热,片刻撤去C处酒精灯.部分实验现象有:①Pt丝继续保持红热,②E中Cu片慢慢溶解.回答下列问题:
科研小组为探究氮的化合物性质,按如图连接好装置,进行实验.将C处Pt丝加热至红热,再将A试管中物质加热,片刻撤去C处酒精灯.部分实验现象有:①Pt丝继续保持红热,②E中Cu片慢慢溶解.回答下列问题: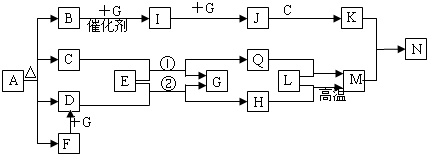
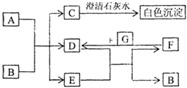 图中A~G均为中学化学中常见的物质,它们之间有如下转化关系.其中A、G为非金属单质,A为黑色固体、G为气态;D、F都是大气污染物,主要来源于汽车尾气,而且D为红棕色.请回答以下问题:
图中A~G均为中学化学中常见的物质,它们之间有如下转化关系.其中A、G为非金属单质,A为黑色固体、G为气态;D、F都是大气污染物,主要来源于汽车尾气,而且D为红棕色.请回答以下问题: