题目内容
【题目】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( )
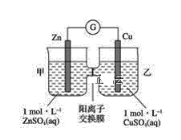
A. 铜电极上发生氧化反应
B. 电池工作一段时间后,乙池溶液的总质量增加
C. 电池工作一段时间后,甲池的c(SO42-)减小
D. 阴、阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
【答案】B
【解析】
由图象可知,该原电池反应式为:Zn+Cu2+=Zn2++Cu,Zn为负极,发生氧化反应,Cu为正极,发生还原反应。
A.Cu为正极,发生还原反应,故A错误;
B.甲池中的Zn2+通过阳离子交换膜进入乙池,乙池中发生反应:Cu2++2e-=Cu,保持溶液呈电中性,进入乙池的Zn2+与放电的Cu2+的物质的量相等,而Zn的摩尔质量大于Cu,故乙池溶液总质量增大,故B正确;
C.阳离子交换膜只允许阳离子和水分子通过,故两池中c(SO42-)不变,故C错误;
D.甲池中的Zn2+通过阳离子交换膜进入乙池,以保持溶液电荷守恒,阴离子不能通过阳离子交换膜向负极移动,故D错误;
答案选B。

练习册系列答案
相关题目