题目内容
下列有关实验的原理、方法和结论都正确的是
| A.将等体积、等pH的氢氧化钠溶液和氨水分别稀释相同倍数,氨水的pH变化大 |
| B.用CH3COOH溶液作导电性实验,灯光较暗,说明CH3COOH是弱电解质 |
| C.向滴有酚酞的Na2CO3溶液中逐滴加入Ba(NO3)2,红色逐渐褪去,说明Na2CO3溶液中存在水解平衡 |
| D.沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 |
C
试题分析:A项,NH3·H2O是弱电解质,存在电离平衡,因此将等体积、等pH的氢氧化钠溶液和氨水分别稀释相同倍数,氨水的pH变化小;B项,实验原理、方法错误,溶液导电性强弱取决于溶液中离子浓度和离子所带电荷数,而与电解质强弱无关;C项,向滴有酚酞的Na2CO3溶液中逐滴加入Ba(NO3)2,因生成BaCO3沉淀而使溶液中c(CO32-)变小,由红色逐渐褪去可证明水解平衡逆向移动,溶液碱性减弱;D项,胶体不带电。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
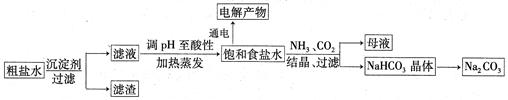
 ,得到纯净的NaCl晶体,需加入以下试剂:
,得到纯净的NaCl晶体,需加入以下试剂: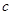 (OH-)的比值是_________。
(OH-)的比值是_________。 NH3·H2O+H+
NH3·H2O+H+ 2NH4+ + SO42-
2NH4+ + SO42- ,电解质通过泵在储罐和电池间循环;离子选择性膜只允许钠离子通过。
,电解质通过泵在储罐和电池间循环;离子选择性膜只允许钠离子通过。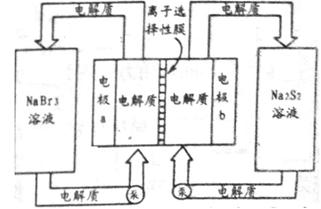
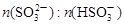 关系如下表:
关系如下表: