题目内容
现有浓度均为0.10mol·L-1的醋酸V1 mL和氢氧化钠溶液V2 mL,下列说法正确的是
| A.常温下,上述溶液中,醋酸溶液的pH=1,氢氧化钠溶液的pH=13 |
| B.常温下,若两溶液混合后pH=7,则混合液:c(Na+)=c(CH3COO-) |
| C.若 V1= V2,将两溶液混合,所得混合液:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| D.V1与V2任意比混合,所得混合液:c (Na+)+ c(H+) =c(OH-)+ c (CH3COO-) |
BD
试题分析:CH3COOH少部分电离,NaOH完全电离,则醋酸溶液的pH>1,故A项错误;常温下pH=7,则溶液中c(H+) =c(OH-),由电荷守恒原理可知,混合液中c(Na+)=c(CH3COO-),故B项正确;由c?V可知,两溶液中酸碱恰好完全中和,得到CH3COONa溶液,由电离、盐类水解可知,c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故C项错误;无论怎样混合,混合液中都只有Na+、H+、OH-、CH3COO-,由电荷守恒原理可知,c (Na+)+ c(H+) =c(OH-)+ c (CH3COO-),故D项错误。

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
 CH3COO-+H+
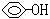
CH3COO-+H+ C6H5O-+H+
C6H5O-+H+ NH4++OH-
NH4++OH-
 )=0.1mol/L的溶液:Na+、Cl-、CO32-、NO3-
)=0.1mol/L的溶液:Na+、Cl-、CO32-、NO3-