题目内容
【题目】下列物质含有共价键的是
A.HClB.MgOC.CaCl2D.KBr
【答案】A
【解析】
一般金属元素与非金属元素形成离子键,非金属元素之间形成共价键,以此来解答。
A. HCl属于共价化合物,只存在共价键,故A可选;
B.MgO属于离子化合物,只存在离子键,故B不选;
C. CaCl2属于离子化合物,只存在离子键,故C不选;
D. KBr属于离子化合物,只存在离子键,故D不选;
故答案选A。

 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案【题目】下图为元素周期表的一部分:
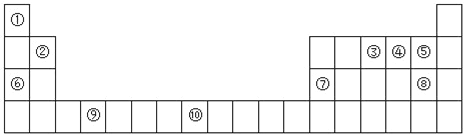
(1)元素③的基态原子轨道表示式为_________________。
(2)元素⑩原子的外围电子排布式为__________。
(3)元素③④⑤的第一电离能由大到小的顺序为___________(填元素符号),其简单离子半径由大到小的顺序为______________(填离子符号)。
(4)⑤与⑧气态氢化物中沸点较高的是_______(填化学式),原因是______________。
(5)以下组合的原子间反应最容易形成离子键的是_____(选填A、B、C、D,下同),最容易形成共价键的是_____,用电子式表示该共价化合物的形成过程______________。
A.和⑤ B.和⑤
C.⑤和⑥ D.⑥和⑧
(6)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的单质及其化合物有相似的性质.写出元素②的最高价氧化物与NaOH溶液反应的离子方程式_________________________________________________。
(7)根据下列五种元素的第一至第四电离能数据(单位:KJ·mol﹣1),回答下面各题:
元素代号 | I1 | I2 | I3 | I4 |
Q | 2080 | 4000 | 6100 | 9400 |
R | 500 | 4600 | 6900 | 9500 |
S | 740 | 1500 | 7700 | 10500 |
T | 580 | 1800 | 2700 | 11600 |
U | 420 | 3100 | 4400 | 5900 |
①在周期表中,最可能处于同一主族的是_________(填元素代号)。
②若T为第三周期元素,则T属于________(填“s”、“p”、“d”、“ds”)区元素,Z是第三周期元素中原子半径最小的主族元素,则T、Z形成的化合物属于__(填“共价”或“离子”)化合物。