题目内容
【题目】用固体NaOH配制一定物质的量浓度的溶液时,下列操作会导致溶液浓度偏高的是
A.在烧杯中溶解时,有少量液体溅出B.样品中含有少量Na2O杂质
C.容量瓶使用前未干D.定容时仰视液面
【答案】B
【解析】
A.在烧杯中溶解时,有少量液体溅出,溶质质量减少,溶液浓度偏低,A不符合题意;
B.样品中含有Na2O杂质,氧化钠与水反应生成氢氧化钠。相同质量的氧化钠、氢氧化钠溶于水,氧化钠的生成的氢氧化钠多,故溶液浓度偏高,B符合题意;
C.容量瓶使用前未干燥对溶液浓度无影响,C不符合题意;
D.定容时仰视液面,导致加入蒸馏水的体积偏大,溶液浓度偏低,D不符合题意。
答案选B。

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
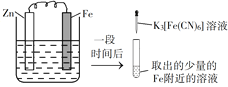
【题目】验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化的3%NaCl溶液)。
① | ② | ③ |
|
|
|
在Fe表面生成蓝色沉淀 | 试管内无明显变化 | 试管内生成蓝色沉淀 |
下列说法不正确的是
A. 对比②③,可以判定Zn保护了Fe
B. 对比①②,K3[Fe(CN)6]可能将Fe氧化
C. 验证Zn保护Fe时不能用①的方法
D. 将Zn换成Cu,用①的方法可判断Fe比Cu活泼