题目内容
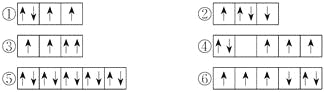
【题目】在焊接铜器时可用NH4Cl溶液除去铜器表面的氧化铜以便焊接,其反应为:CuO+NH4Cl → Cu+CuCl2+N2↑+H2O(未配平)。下列说法正确的是
A. 反应中被氧化和被还原的元素分别为Cu和N
B. 反应中氧化剂和还原剂的物质的量之比为3∶2
C. 反应中产生0.2 mol气体时,转移0.6 mol电子
D. 该反应中被还原的CuO占参与反应CuO的![]()
【答案】B
【解析】
根据CuO+NH4Cl → Cu+CuCl2+N2↑+H2O分析可知:Cu由+2价降低为0,被还原;N元素的化合价由-3价升高为0,被氧化;根据电子守恒、原子守恒配平为4CuO+2NH4Cl = 3Cu+CuCl2+N2↑+4H2O即可判断。
A.氯化铵中N元素化合价升高被氧化,氧化铜中铜元素化合价降低被还原,则被氧化和被还原的元素分别为N和Cu,故A错误;
B.根据反应4CuO+2NH4Cl=3Cu+CuCl2+N2↑+4H2O可知,参加反应的氧化剂为氧化铜,还原剂为氯化铵,作氧化剂的氧化铜与作还原剂的氯化铵的物质的量之比为3:2,故B正确;
C.由反应可知,生成1mol气体转移6mol电子,则产生0.2mol的气体转移的电子为0.2mol×6=1.2mol,故C错误;
D.由反应4CuO+2NH4Cl=3Cu+CuCl2+N2+4H2O可知,被还原的氧化铜占参加反应的氧化铜的3/4,故D错误。
综上所述,本题正确答案为B。

【题目】某化学学习小组用酸性KMnO4溶液与H2C2O4(K1 = 5.4 × 10-2)的反应(此反应为放热反应)进行如下实验:
Ⅰ、探究“条件对化学反应速率的影响”,并设计了如下的方案记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20 molL-1 H2C2O4溶液、0.010 molL-1 KMnO4 溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽
物理量 | V(H2C2O4溶液)/mL | V(蒸馏水)/mL | V(KMnO4溶液)/mL | T/℃ | 乙 |
① | 2.0 | 0 | 4.0 | 50 | |
② | 2.0 | 0 | 4.0 | 25 | |
③ | 2.0 | a | 4.0 | 25 |
(1)完成该反应的实验原理: + MnO4- + = CO2↑ + Mn2+ + H2O_______________
(2)上述实验①、②是探究___________对化学反应速率的影响;若上述实验②、③是探究浓度对化学反应速率的影响,则 a 为___________;乙是实验需要测量的物理量,则表格中“乙”应填写_______________。
Ⅱ、测定H2C2O4xH2O中x值。已知:M(H2C2O4) = 90 gmol-1。①称取1.260 g 纯草酸晶体,将草酸制成 100.00 mL 水溶液为待测液; ②取 25.00 mL 待测液放入锥形瓶中,再加入适量的稀 H2SO4; ③用浓度为 0.05 000 molL-1的KMnO4标准溶液进行滴定。
(1)某学生的滴定方式(夹持部分略去)如下,最合理的是________(选填 a、b)。由图可知消耗 KMnO4 溶液体积为________ mL。

(2)滴定终点锥形瓶内现象为__________________________________________________。
(3)通过上述数据,求得 x =______________。
(4)下列操作会造成所测x偏大的是____________(填字母)。
A.滴定终点俯视读数
B.锥形瓶用待测溶液润洗
C.滴定前有气泡,滴定后没有气泡
D.配制100 mL待测溶液时,有少量溅出