��Ŀ����
|
ǿ���ǿ����ϡ��Һ�е��к��ȿɱ�ʾΪH+(aq)��OH��(aq) HNO3(aq)��KOH(aq) | |
A�� |
Q1��Q2��Q3 |
B�� |
Q2��Q1��Q3 |
C�� |
Q2��Q3��Q1 |
D�� |
Q2��Q3��Q1 |
�𰸣�C
������
������
|
��������к�ʱҪ�������ȣ�����Q1��57.3 kJ/mol��Ũ�����к�ʱҪϡ�ͷų�������Q2��57.3 kJ/mol�����ķ�Ӧ�����к��ȣ�Q3��57.3 kJ/mol������Q2��Q3��Q1�� |

��ϰ��ϵ�д�
�����Ŀ
ǿ���ǿ����ϡ��Һ�е��к��ȿɱ�ʾΪ��
H+��aq��+OH-��aq���TH2O��l������H=-57.3KJ/mol����֪����Һ�з�Ӧ�У�
CH3COOH��aq��+NaOH��aq���TCH3COONa��aq��+H2O��l������H=-Q1 KJ/mol
H2SO4��aq��+NaOH��aq���T
Na2SO4��aq��+H2O��l������H=-Q2 KJ/mol
HCl��aq��+NaOH��aq���TNaCl��aq��+H2O��l������H=-Q3 KJ/mol
��Q1��Q2��Q3�Ĺ�ϵ��ȷ���ǣ�������
H+��aq��+OH-��aq���TH2O��l������H=-57.3KJ/mol����֪����Һ�з�Ӧ�У�
CH3COOH��aq��+NaOH��aq���TCH3COONa��aq��+H2O��l������H=-Q1 KJ/mol
| 1 |
| 2 |
| 1 |
| 2 |
HCl��aq��+NaOH��aq���TNaCl��aq��+H2O��l������H=-Q3 KJ/mol
��Q1��Q2��Q3�Ĺ�ϵ��ȷ���ǣ�������
| A��Q1=Q2=Q3 |
| B��Q2��Q3��Q1 |
| C��Q2��Q1��Q3 |
| D��Q2=Q3��Q1 |
ǿ���ǿ����ϡ��Һ�е��к��ȿɱ�ʾΪ��H+��aq��+OH-��aq��=H2O��l������H=-57.3k kJ?mol-1����֪����Һ�з�Ӧ�У�CH3COOH��aq��+NaOH��aq��=CH3COONa��aq��+H2O��l������H1=-Q1kJ?mol-1��
H2SO4��Ũ��+NaOH��aq��=
Na2SO4��aq��+H2O��l������H2=-Q2 kJ?mol-1
HNO3��aq��+KOH��aq��=KNO3��aq��+H2O��l������H3=-Q3 kJ?mol-1��
���H1����H2����H3�Ĺ�ϵ��ȷ���ǣ�������
| 1 |
| 2 |
| 1 |
| 2 |
HNO3��aq��+KOH��aq��=KNO3��aq��+H2O��l������H3=-Q3 kJ?mol-1��
���H1����H2����H3�Ĺ�ϵ��ȷ���ǣ�������
| A����H1=��H2=��H3 |
| B����H2����H1����H3 |
| C����H1����H3����H2 |
| D����H2=��H3����H1 |
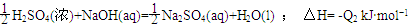
 KNO3��aq��+H2O(l) ; ��H= -Q3 kJ��mol-1��
KNO3��aq��+H2O(l) ; ��H= -Q3 kJ��mol-1��