题目内容
16.现有下列试剂:①蒸馏水;②AgNO3溶液;③BaCl2溶液;④稀盐酸,欲检验硝酸钠固体中是否含有少量可溶性硫酸盐杂质,应选用的试剂是( )| A. | ①③④ | B. | ②④ | C. | ③④ | D. | ①②③ |
分析 检验硝酸钠固体中是否含有少量可溶性硫酸盐杂质,可取少量固体溶于水,先加盐酸排除银离子等干扰,再加氯化钡,若生成白色沉淀,含硫酸盐,以此来解答.
解答 解:检验硝酸钠固体中是否含有少量可溶性硫酸盐杂质,选试剂为①蒸馏水、④稀盐酸、③BaCl2溶液,即固体溶于水,先加盐酸排除银离子等干扰,再加氯化钡,若生成白色沉淀,含硫酸盐,
故选A.
点评 本题考查物质的检验和鉴别,为高频考点,把握硫酸根离子的检验方法为解答的关键,注意检验时应排除干扰离子,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
7.下列实验操作中,主要是从安全因素考虑的是( )
a.点燃可燃性气体前检验气体纯度
b.给试管里的液体加热时,试管口应略向上倾斜,外壁干燥后再预热
c.给试管里的固体加热时,试管口应略向下倾斜,外壁干燥后再预热
d.用氢气还原氧化铜时,应先通一会儿氢气,再加热氧化铜
e.实验室用高锰酸钾制氧气结束时,先从水槽中移出导气管,再熄灭酒精灯.
a.点燃可燃性气体前检验气体纯度
b.给试管里的液体加热时,试管口应略向上倾斜,外壁干燥后再预热
c.给试管里的固体加热时,试管口应略向下倾斜,外壁干燥后再预热
d.用氢气还原氧化铜时,应先通一会儿氢气,再加热氧化铜
e.实验室用高锰酸钾制氧气结束时,先从水槽中移出导气管,再熄灭酒精灯.
| A. | abc | B. | ade | C. | dce | D. | 全部 |
11.VL K2SO4溶液中,含有K+mg,则溶液中SO42-的物质的量浓度为( )
| A. | $\frac{39m}{V}$mol•L-1 | B. | $\frac{2m}{39V}$mol•L-1 | C. | $\frac{m}{39V}$mol•L-1 | D. | $\frac{m}{78V}$mol•L-1 |
4.用以下三种途径来制取相等质量的硝酸铜:(1)铜跟浓硝酸反应;(2)铜跟稀硝酸反应;(3)铜先跟氧气反应生成氧化铜,氧化铜再跟硝酸反应.以下叙述中正确的是( )
| A. | 三种途径所消耗的铜的物质的量相等 | |
| B. | 三种途径所消耗的硝酸的物质的量相等 | |
| C. | 所消耗的铜的物质的量是:途径(3)>途径(1)>途径(2) | |
| D. | 所消耗的硝酸的物质的量是:途径(1)>途径(2)>途径(3) |
1. 正丁醚是惰性溶剂,可用作有机合成反应溶剂.某实验小组利用如下装置(夹持和加热装置均省略)合成正丁醚.发生的反应为:
正丁醚是惰性溶剂,可用作有机合成反应溶剂.某实验小组利用如下装置(夹持和加热装置均省略)合成正丁醚.发生的反应为:
2CH3CH2CH2CH2OH$\stackrel{H_{2}SO_{4}}{→}$CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
反应物和产物的相关数据列表如下:
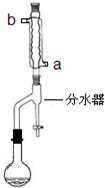
实验步骤:在一定容积的三口烧瓶中,加入10.9g(相当13.5mL)正丁醇、2.5mL浓硫酸和几粒沸石,摇匀后,一口装上温度计,温度计插入液面以下,另一口装上分水器,分水器的上端接球形冷凝管,先在分水器内放置1.7mL水,另一口用塞子塞紧.然后将三口瓶放在石棉网上小火加热至微沸,进行分水.反应中产生的水经球形冷凝管后,收集在分水器的下层,上层有机层积至分水器支管时,即可返回烧瓶.大约经1.5h后,三口瓶中反应液温度可达134一136℃,当下层水至分水器的支管口处停止反应.
将反应液冷却到室温后倒入盛有25mL水的分液漏斗中,经过分离、洗涤后再分离提纯可得正丁醚3.4g.回答下列问题:
(1)该实验时球形冷凝管的进水口为2(填1或2);
(2)在该实验中,三口烧瓶的容积最适合的是A(填入正确选项前的字母).
A.50mL B.150mL C.250mL D.500mL
(3)本实验中容易产生烃类化合物的化学反应方程式为:HOCH2CHBrCH2CH3 $→_{△}^{浓H_{2}SO_{4}}$CH2=CHCH2CH3+H2O.
(4)反应液冷却到室温后倒入盛有25mL水的分液漏斗中,振荡静置,得到有机层的操作方法是将分液漏斗颈上的玻璃塞打开,再将分液漏斗下面活塞拧开,使下层液体慢慢沿烧杯壁留下,关闭分液漏斗,将上层有机物从分液漏斗上口倒出.
(5)有机层粗产物依次用12mL水、8mL5%氢氧化钠溶液、8mL水和8mL饱和氯化钙溶液洗涤.用氢氧化钠溶液溶液洗涤的目的是除去产品中的硫酸;用氯化钙溶液洗涤的目的是除去少量的氢氧化钠,且能减少产物的损失.
(6)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是cba(填字母).
a.蒸馏 b.过滤 c.加入无水CaCl2
(7)本实验所得到的正丁醚产率为35.34%.
 正丁醚是惰性溶剂,可用作有机合成反应溶剂.某实验小组利用如下装置(夹持和加热装置均省略)合成正丁醚.发生的反应为:
正丁醚是惰性溶剂,可用作有机合成反应溶剂.某实验小组利用如下装置(夹持和加热装置均省略)合成正丁醚.发生的反应为:2CH3CH2CH2CH2OH$\stackrel{H_{2}SO_{4}}{→}$CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
反应物和产物的相关数据列表如下:
| 化合物 名称 | 密度(g/mL ) | 熔 点(℃) | 沸 点(℃) | 水中溶解性 |
| 正丁醇 | 0.810 | -89.8 | 118.0 | 微溶 |
| 正丁醚 | 0.7689 | -95.3 | 142 | 不溶于水 |
| 备注:正丁醚微溶于饱和氯化钙溶液. | ||||
将反应液冷却到室温后倒入盛有25mL水的分液漏斗中,经过分离、洗涤后再分离提纯可得正丁醚3.4g.回答下列问题:
(1)该实验时球形冷凝管的进水口为2(填1或2);
(2)在该实验中,三口烧瓶的容积最适合的是A(填入正确选项前的字母).
A.50mL B.150mL C.250mL D.500mL
(3)本实验中容易产生烃类化合物的化学反应方程式为:HOCH2CHBrCH2CH3 $→_{△}^{浓H_{2}SO_{4}}$CH2=CHCH2CH3+H2O.
(4)反应液冷却到室温后倒入盛有25mL水的分液漏斗中,振荡静置,得到有机层的操作方法是将分液漏斗颈上的玻璃塞打开,再将分液漏斗下面活塞拧开,使下层液体慢慢沿烧杯壁留下,关闭分液漏斗,将上层有机物从分液漏斗上口倒出.
(5)有机层粗产物依次用12mL水、8mL5%氢氧化钠溶液、8mL水和8mL饱和氯化钙溶液洗涤.用氢氧化钠溶液溶液洗涤的目的是除去产品中的硫酸;用氯化钙溶液洗涤的目的是除去少量的氢氧化钠,且能减少产物的损失.
(6)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是cba(填字母).
a.蒸馏 b.过滤 c.加入无水CaCl2
(7)本实验所得到的正丁醚产率为35.34%.
 在苹果、香蕉等水果的果香中存在着乙酸正丁酯.某化学课外兴趣小组欲以乙酸和正丁醇为原料合成乙酸正丁酯.
在苹果、香蕉等水果的果香中存在着乙酸正丁酯.某化学课外兴趣小组欲以乙酸和正丁醇为原料合成乙酸正丁酯.