题目内容
(15分)下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用化学用语
回答下列问题:
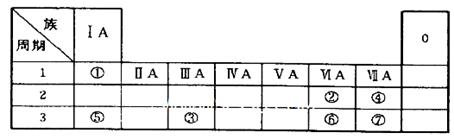
(1)④、⑤、⑦的原子半径由大到小的顺序为_______(用元素符号表示,下同)。
(2)⑥和⑦的最高价含氧酸的酸性强弱为_______>_______。
(3)①、②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe+氧化,写出该反应的离子方程式_______。
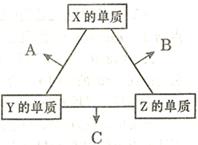
(4)由表中元素形成的物质可发生如图中的反应,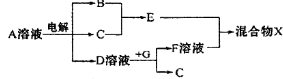
其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。
①写出D溶液与G反应的化学方程式______________.
②写出检验A溶液中溶质的阴离子的方法:______________.
③常温下,若电解1 L 0.1 mol/L的A溶液,一段时间后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为_______mol。
④若上图中各步反应均为恰好完全转化,则混合物X中含有的物质有_______ 。
回答下列问题:

(1)④、⑤、⑦的原子半径由大到小的顺序为_______(用元素符号表示,下同)。
(2)⑥和⑦的最高价含氧酸的酸性强弱为_______>_______。
(3)①、②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe+氧化,写出该反应的离子方程式_______。
(4)由表中元素形成的物质可发生如图中的反应,

其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。
①写出D溶液与G反应的化学方程式______________.
②写出检验A溶液中溶质的阴离子的方法:______________.
③常温下,若电解1 L 0.1 mol/L的A溶液,一段时间后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为_______mol。
④若上图中各步反应均为恰好完全转化,则混合物X中含有的物质有_______ 。
(1) Na>Cl>F ; (2)HClO4>H2SO4 ; (3)H2O2+2Fe2++2H+=2Fe3++2H2O
(4) ①2Al+2NaOH+2H2O=2NaAlO2+3H2↑ ; ②取少量A溶液滴加几滴(稀硝酸酸化的)硝酸银溶液有白色沉淀生成; ③0.01; ④Al(OH)3 H2O NaCl。
(4) ①2Al+2NaOH+2H2O=2NaAlO2+3H2↑ ; ②取少量A溶液滴加几滴(稀硝酸酸化的)硝酸银溶液有白色沉淀生成; ③0.01; ④Al(OH)3 H2O NaCl。
试题分析:根据元素在周期表中的位置可推知:①的H;②是O;③是Al;④是F;⑤是Na;⑥是S;⑦是Cl。(1)同一周期的元素,原子序数越小,原子半径越大;不同周期的元素,原子核外电子层数越多,原子半径就越大。所以这几种元素的原子半径由大到小的顺序为Na>Cl>F;(2)元素的非金属性Cl>S.元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强,所以S、Cl的最高价含氧酸的酸性强弱为HClO4>H2SO4;(3) H2O2在酸性溶液中能将Fe+氧化,该反应的离子方程式是H2O2+2Fe2++2H+=2Fe3++2H2O;(4)根据图示个物质的关系可知:A是NaCl ;B是Cl2;C是H2;D是NaOH;E是HCl;G是Al;F是NaAlO2;X是NaCl与AlCl3的混合物。①NaOH溶液与Al单质反应的化学方程式是2Al+2NaOH+2H2O=2NaAlO2+3H2↑;②检验Cl-的方法是取少量A溶液滴加几滴(稀硝酸酸化的)硝酸银溶液有白色沉淀生成,就证明含有Cl-;③NaCl溶液电解的方程式是:2NaCl+2H2O
 Cl2↑+H2↑+2NaOH 。pH=12,c(NaOH) =0.01mol/L,n(NaOH)=0.01mol。根据反应方程式可知:每产生1mol的NaOH,单质转移1mol。由于产生了0.01mol的NaOH,所以转移电子0.01mol。④若上图中各步反应均为恰好完全转化,假设有2mol的NaCl,则产生NaOH为2mol;Cl2和H2都是1mol.二者反应得到的HCl是2mol; NaOH发生反应2Al+2NaOH+2H2O=2NaAlO2+3H2↑得到2mol的NaAlO2。在发生反应:NaAlO2+HCl+H2O = Al(OH)3↓+NaCl。所以混合物X中含有的物质有Al(OH)3、NaCl、H2O.
Cl2↑+H2↑+2NaOH 。pH=12,c(NaOH) =0.01mol/L,n(NaOH)=0.01mol。根据反应方程式可知:每产生1mol的NaOH,单质转移1mol。由于产生了0.01mol的NaOH,所以转移电子0.01mol。④若上图中各步反应均为恰好完全转化,假设有2mol的NaCl,则产生NaOH为2mol;Cl2和H2都是1mol.二者反应得到的HCl是2mol; NaOH发生反应2Al+2NaOH+2H2O=2NaAlO2+3H2↑得到2mol的NaAlO2。在发生反应:NaAlO2+HCl+H2O = Al(OH)3↓+NaCl。所以混合物X中含有的物质有Al(OH)3、NaCl、H2O.
练习册系列答案
相关题目